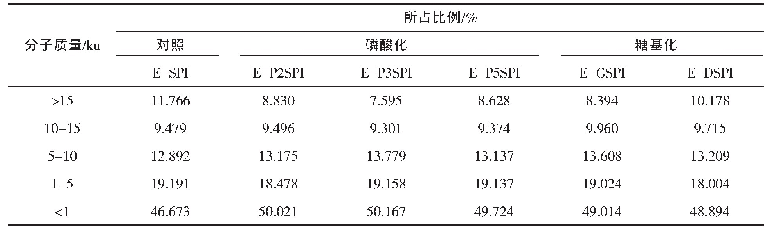
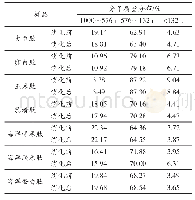
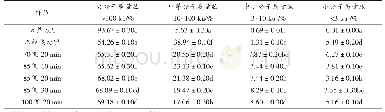
《表1 不同热处理条件下SPI消化产物中蛋白分子质量分布》
 提示:宽带有限、当前游客访问压缩模式
提示:宽带有限、当前游客访问压缩模式
本系列图表出处文件名:随高清版一同展现
《不同热处理条件下大豆蛋白体外模拟消化产物结构和分子质量分布》
注:同列中不同字母(a-f)表示P<0.05水平的差异显著性。
体积排阻-凝胶色谱(SEC-HPLC)主要是根据多孔凝胶对不同分子大小蛋白质的不同排阻效应进行分离,从而测定蛋白质分子质量[26]。天然SPI的Superdex 200凝胶洗脱图谱和蛋白质分子质量分布标准曲线如图5所示。其标样曲线的回归方程为y=-0.0796x+6.5721,R2=0.9891。根据该回归方程的保留时间估算出蛋白质的分子质量[27]。表1为不同热处理条件下SPI消化产物的分子质量分布。与天然SPI相比,未经热处理的SPI消化产物中大分子质量肽(>100 ku)的含量显著降低(P<0.05),中等分子质量肽(10~100 ku)和小分子质量肽(<3 ku)的含量显著增加(P<0.05),而中小分子质量肽(3~10 ku)的含量变化不显著(P>0.05),这说明胃蛋白酶能够将大分子SPI消化降解成小分子肽。与未经热处理的SPI消化产物相比,升高热处理温度或延长热处理时间虽会增加大分子质量肽(>100 ku)和中小分子质量肽(3~10ku)的含量,但会降低中等分子质量肽(10~100ku)和小分子质量肽(<3 ku)的含量,这说明热处理改变SPI消化产物的分子质量分布。这可能是由于热变性导致SPI结构伸展,促进了可溶性和不溶性聚集体的形成[28]。胃蛋白酶消化降解这些变性蛋白形成的聚集体时,主要生成大分子质量肽,而小分子质量肽及氨基酸释放较少。Iung等[29]在对β-乳球蛋白的消化性研究中发现,采用胰蛋白酶水解β-乳球蛋白会产生较多小分子质量肽,而消化热处理的β-乳球蛋白则会产生较多大分子质量肽,这与本研究结果相似。
| 图表编号 | XD00179302900 严禁用于非法目的 |
|---|---|
| 绘制时间 | 2020.05.31 |
| 作者 | 赵城彬、尹欢欢、鄢健楠、刘景圣、杜琛、牛希、齐宝坤 |
| 绘制单位 | 吉林农业大学食品科学与工程学院小麦和玉米深加工国家工程实验室、吉林农业大学食品科学与工程学院小麦和玉米深加工国家工程实验室、吉林农业大学食品科学与工程学院小麦和玉米深加工国家工程实验室、吉林农业大学食品科学与工程学院小麦和玉米深加工国家工程实验室、吉林农业大学食品科学与工程学院小麦和玉米深加工国家工程实验室、吉林农业大学食品科学与工程学院小麦和玉米深加工国家工程实验室、东北农业大学食品学院 |
| 更多格式 | 高清、无水印(增值服务) |