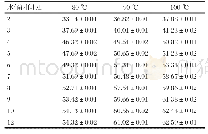
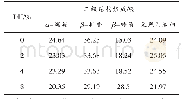
《表2 不同水解度的大米蛋白的热力学行为》
 提示:宽带有限、当前游客访问压缩模式
提示:宽带有限、当前游客访问压缩模式
本系列图表出处文件名:随高清版一同展现
《限制性酶解对大米蛋白结构、功能特性及体外抗氧化活性的影响》
注:结果表示为平均值±方差,字母相异表示差异性显著(P<0.05)。
不同水解度的大米蛋白的热力学特性如表2所示。样品在升温的过程中,由于涉及蛋白质间新的分子键的生成和分子内的折叠与解折叠,因此出现变性温度和焓的变化。当水解度为2%和4%时,蛋白的变性温度相比于天然大米蛋白有所提高,说明适度的水解可以提高蛋白的热稳定性,扩大蛋白的应用范围;而当水解度为8%时,蛋白的变性温度降至80.30℃,此时的DSC图谱没有明显的吸热峰(数据未显示),表明过度水解会破坏蛋白内和蛋白间维持结构稳定的氢键,加剧蛋白分子间的聚集,进而导致蛋白质的耐热性降低。
| 图表编号 | XD00201333600 严禁用于非法目的 |
|---|---|
| 绘制时间 | 2020.11.30 |
| 作者 | 马晓雨、陈先鑫、胡振瀛、朱雪梅、熊华、赵强 |
| 绘制单位 | 南昌大学食品科学与技术国家重点实验室、山东科技大学泰山科技学院、江西卫生职业学院、南昌大学食品科学与技术国家重点实验室、南昌大学食品科学与技术国家重点实验室、大连工业大学食品学院、南昌大学食品科学与技术国家重点实验室、南昌大学食品科学与技术国家重点实验室 |
| 更多格式 | 高清、无水印(增值服务) |