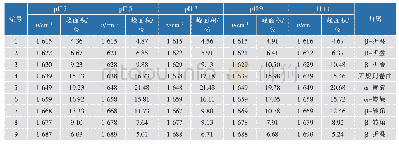
《表1 利用酰胺I带拟合SPI二级结构结果》
 提示:宽带有限、当前游客访问压缩模式
提示:宽带有限、当前游客访问压缩模式
本系列图表出处文件名:随高清版一同展现
《工业改性对大豆蛋白结构及大豆蛋白-肌原纤维蛋白复合凝胶的影响》
注:同列不同字母表示样品间差异显著(P<0.05)。下表同。
由表1可知,4种工业改性处理均减少了SPI的α-螺旋和无规卷曲结构相对含量,并增加了β-折叠与β-转角结构相对含量。本团队前期研究报道了与未经热处理的SPI相比,热处理30 min增加了SPI的α-螺旋结构含量,降低了β-折叠结构含量[21]。本实验中工业热改性是在81℃的闪蒸温度下短时加热,由此推测工业热改性与实验室热改性之间的差异会造成SPI二级结构的不同转变。耿蕊[22]研究表明碱改性会降低SPI的α-螺旋结构含量,暴露出更多的疏水基团。布冠好等[23]报道了SPI经糖基化后,复合蛋白质的α-螺旋含量降低,β-折叠结构含量增加。SPI经氧化后,α-螺旋和无规卷曲含量下降,β结构含量上升;卢岩[24]研究证实了SPI氧化过程中伴随着α-螺旋结构的损失。
| 图表编号 | XD00123393000 严禁用于非法目的 |
|---|---|
| 绘制时间 | 2020.02.25 |
| 作者 | 贾子璇、冉安琪、刘季善、李杨、王中江、江连洲 |
| 绘制单位 | 东北农业大学食品学院、东北农业大学食品学院、山东万得福实业集团有限公司、东北农业大学食品学院、东北农业大学食品学院、东北农业大学食品学院 |
| 更多格式 | 高清、无水印(增值服务) |