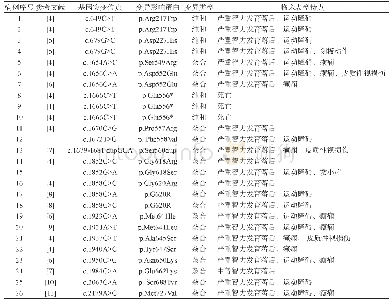
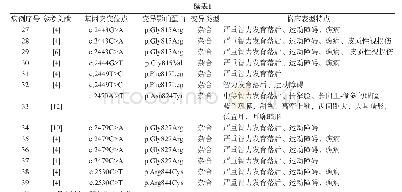
《表1 ZMPSTE24基因突变致4种疾病类型的临床表型总结与比较》
 提示:宽带有限、当前游客访问压缩模式
提示:宽带有限、当前游客访问压缩模式
本系列图表出处文件名:随高清版一同展现
《ZM PSTE24基因突变致限制性皮病1例病例报告并文献复习》
注RD:限制性皮病;HGPS:Hutchinson-Gilford早老综合征;MADB:下颌骨发育不良伴B型脂肪代谢障碍;MS:代谢综合征
总结已报道的64例患儿ZMPSTE24基因突变和临床表型,可发现基因型与表型关系密切。表1显示,ZMPSTE24基因突变可导致4种截然不同的临床表型。虽然50%以上的病例可表现为特征性皮肤改变、早产、低体重儿、呼吸困难、异常面容、骨骼发育不良和关节挛缩僵硬等多系统累及,但在4种表型中,RD患儿表型最为严重。RD主要表现为胎膜早破、宫内生长受限、胎动少、早产、低体重、呼吸困难、皮肤异常、异常面容、骨骼发育不良和关节僵硬挛缩的10种表型。除胎膜早破(37/49)和骨骼发育不良(48/49)外,其他8种表型的外显率均为100%。49例RD患儿均于婴儿期死亡,存活时间最长为56 d[8]。HGPS在胎儿期无明显异常,仅1例为早产,其主要表现为生后逐渐呈现的皮肤、骨关节早老性表现和发育迟缓。目前报道的2例HGPS患儿分别于10周龄和4月龄出现皮肤紧绷、关节活动受限等表现,后逐渐加重,其中1例患儿于2岁9月龄死亡[30]。MADB在胎儿期的生长和运动无异常,但表现为不同比例的RD和HGPS的表型。12例MADB患者最早发病年龄为5月龄[25],未成年患儿9例,年龄范围为5月龄至16岁;成年患者3例,平均年龄为30岁。目前报道的1例47岁MS患者,表现为2型糖尿病、脂类代谢障碍导致的肥胖[31]。其次,ZMPSTE24基因突变类型在不同疾病中明显不同。Agarwal等[26]研究发现,ZMPSTE24基因发生双等位无效突变时,临床表现为RD或HGPS。而ZMPSTE24基因发生框内突变时,临床表现为MADB或MS。Barrowman等[34]提出ZMPSTE24突变的临床表型,其严重程度与ZMPATE24的蛋白产物锌金属蛋白酶活性和核纤层蛋白A前体(prelamin A)的堆积程度相关。核纤层蛋白A前体需经锌金属蛋白酶加工修饰才能形成成熟的lamin A。当ZMPATE24基因突变,核纤层蛋白A前体堆积,导致核膜皱褶或凹陷,影响lamin A蛋白功能,导致一系列疾病表型[32]。在49例RD患儿中,47例为ZMPSTE24基因的双等位基因无效突变。其中,Leu362Phefs*19出现在30例患儿中,26例为纯合突变,4例为复合杂合突变,突变频率高达57.1%(56/98),为热点突变[7]。本文患儿也是该突变位点的纯合突变。在12例MADB患儿中,9例为ZMPSTE24基因无效/框内突变,另3例为纯合错义突变(L425P、Y399C、L94P)。Barrowman等[34]认为,MADB患儿ZMPSTE24基因至少有一个等位基因是框内突变,可部分保存Zmpste24活性。另外,L425P突变发生于ZMPSTE24基因酶活性区域,L94P和Y399C突变位于Zmpste24腔形结构的底部,这些部位突变可影响酶活性,导致MADB[33,35]。1例RD患儿的无效/框内突变(Q41Ter;R465G)[1],因R465G位于锌金属蛋白酶活性区域的MH6结构域上,影响酶活性,表型严重。Denecke等[29]报道1例患儿ZMPSTE24基因虽然发生纯合无效突变(c.1204-4_1216del17,p.V402SfsTer403),但因其合并LMNA基因单杂合错义突变(c.1960C>T,p.R654X),核纤层蛋白A前体产生减少,临床表型为HGPS。Agarwal等[24]报道1例澳大利亚患者为N265S和L362F(fs X18)突变,临床表型为MADB。但是,同样是N265S和L362F(fs X18)突变的1例英国患者,临床表型却很复杂,综合了RD、HGPS和MADB的表型,临床诊断为HGPS[30],说明基因型与表型的复杂性。
| 图表编号 | XD00113037000 严禁用于非法目的 |
|---|---|
| 绘制时间 | 2019.08.25 |
| 作者 | 赵得雄、王晴、彭小敏、海妤婷、马力刚、汪悦、王生兰、王慧君、吴冰冰 |
| 绘制单位 | 青海红十字医院产科、复旦大学附属儿科医院上海市出生缺陷防治重点实验室复旦大学儿童发育与疾病转化医学中心、复旦大学附属儿科医院上海市出生缺陷防治重点实验室复旦大学儿童发育与疾病转化医学中心、青海红十字医院产科、青海红十字医院产科、复旦大学附属儿科医院上海市出生缺陷防治重点实验室复旦大学儿童发育与疾病转化医学中心、青海红十字医院产科、复旦大学附属儿科医院上海市出生缺陷防治重点实验室复旦大学儿童发育与疾病转化医学中心、复旦大学附属儿科医院上海市出生缺陷防治重点实验室复旦大学儿童发育与疾病转化医学中心 |
| 更多格式 | 高清、无水印(增值服务) |
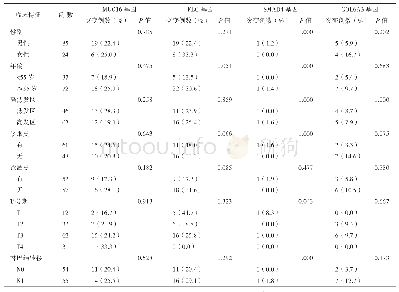
![表1 3组临床资料、基因突变频率、主要基因突变类型比较[n(%)]](http://bookimg.mtoou.info/tubiao/gif/YXYQ202012005_02200.gif)
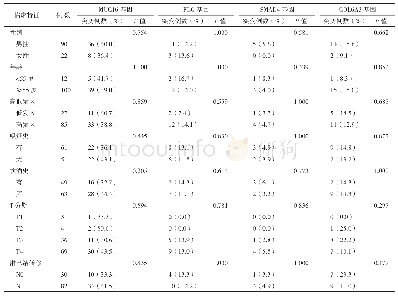
![表1 MUT和MMACHC基因缺陷致MMA临床表型比较[n(%)]](http://bookimg.mtoou.info/tubiao/gif/XZEK202006012_02700.gif)