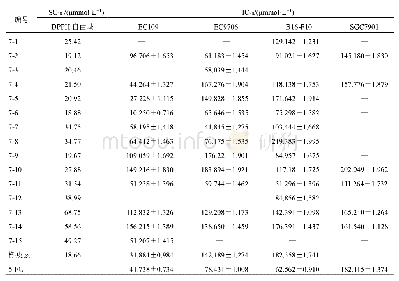
《表1 0 N-酰基-甘氨酸-2-氰基吡咯烷衍生物对FAP抑制IC50》
Ryabtsova等[87]基于N-酰基-甘氨酸-2-氰基吡咯烷骨架(图4),通过引入不同酰类取代基并检测其衍生物对二肽基肽酶的抑制作用,研究了不同取代基衍生物对靶酶的构效关系.在固定R2取代基为氢原子时,1-萘甲酰基取代衍生物为最优势构象,但大多数芳香类酰基(不论单环或多环)衍生物对FAP和PREP都有很强的亲和力,而对二肽基肽酶其他成员几乎没有抑制,这说明游离氨基端的阻滞对二肽基肽酶的外肽酶活性作用明显.而2-氰基吡咯烷(R2)C-4位不同取代基衍生物的研究表明,氟原子的引入能在不影响二肽基肽酶家族其他成员的情况下,大幅增强化合物对FAP和PREP的亲和力,更多氟原子能加强FAP抑制作用并减弱PRER的抑制,但作用皆不明显.在此实验的基础上,Jansen等[88]通过引入喹啉酰基,增强了对FAP的亲和力和选择性(IC50约为PREP的83倍)(表10),并研究了喹啉环上氮的不同位置对其抑制作用的影响,确立了N-(4-喹啉酰基)-甘氨酸-(2-氰基吡咯烷)为最优势构象.值得注意的是,相比于N-(4-喹啉酰基)-甘氨酸-(2-氰基吡咯烷),喹啉环C-6位氯原子或溴原子的引入没有明显改变FAP亲和力,但它们确实具有适度增加对PREP的选择性.
| 图表编号 | XD00122706700 严禁用于非法目的 |
|---|---|
| 绘制时间 | 2020.01.20 |
| 作者 | 孙朝晖、邹立伟、杨凌 |
| 绘制单位 | 上海中医药大学交叉科学研究院、上海中医药大学交叉科学研究院、上海中医药大学交叉科学研究院 |
| 更多格式 | 高清、无水印(增值服务) |
 提示:宽带有限、当前游客访问压缩模式
提示:宽带有限、当前游客访问压缩模式