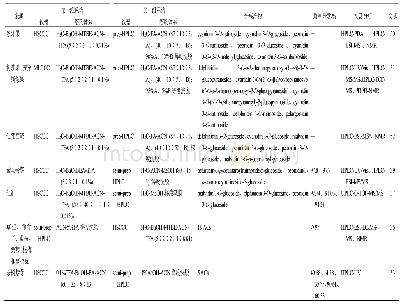
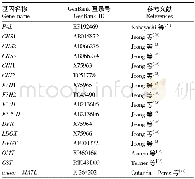
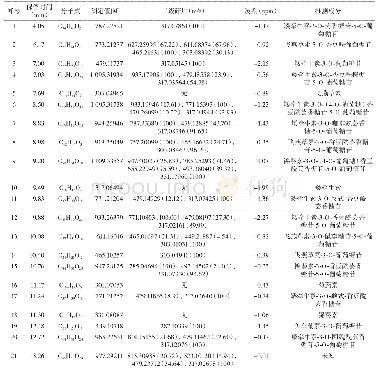
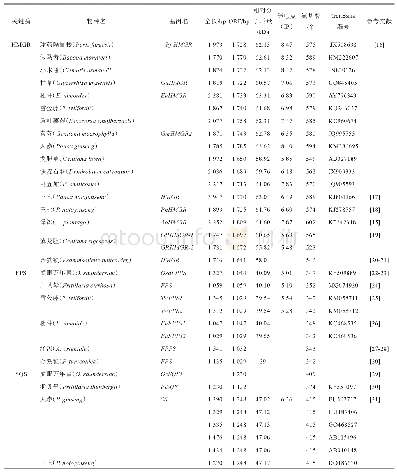
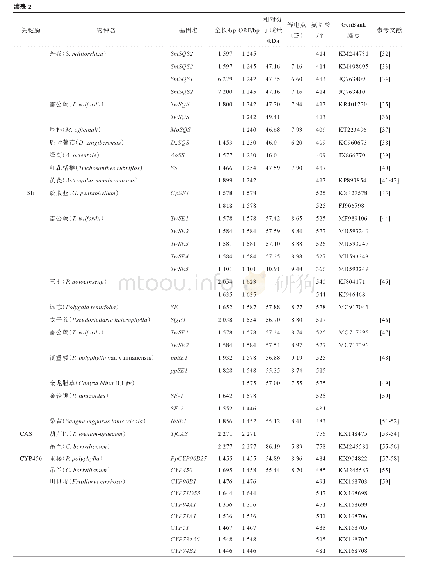
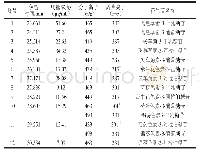
《表1 2010—2019年部分LLC纯化的天然花色苷》
 提示:宽带有限、当前游客访问压缩模式
提示:宽带有限、当前游客访问压缩模式
本系列图表出处文件名:随高清版一同展现
《液液分配色谱及其与液相色谱联用分离天然花色苷的研究进展》
众所周知,选择合适的溶剂体系对LLC分离至关重要。花色苷多具极性,因此分离纯化花色苷多采用极性较强的溶剂体系,常用正丁醇(BuOH)和水作为两相基本溶剂,同时因为花色苷在较低p H值(pH<2)下以稳定的花色阳离子形式,因此溶剂体系中也常有三氟乙酸(TFA)[15]。研究中用来分离花色苷最常用的溶剂体系由水、BuOH、甲基叔丁基醚(MTBE)、乙腈(ACN)及其少量TFA组成(表1),TFA的溶剂浓度0.01%~0.1%不等[32-33],收集目标组分时可于40℃条件下真空浓缩至小体积,氮吹10 min以除去残留的TFA[19]。花色苷极性大且彼此相似,两项溶剂的选择非常关键。目标化合物在两相溶剂中的分配系数(K)是逆流色谱中的一个重要参数,范围一般为0.5~2。K值太小得到的分离度常不理想,而K值过大往往导致样品峰过度展宽和洗脱时间过长。因为Bu OH对整个溶剂体系的极性贡献最大,所以可以通过改变BuOH的比例来调整溶剂体系的极性,且不同花色苷单体性质各不相同,实际应用中要结合具体目标化合物的性质对溶剂体系进行筛选和调整。研究表明,适当调高BuOH比例的溶剂体系,更有利于极性较弱的酰基化花色苷单体的分离[34]。如Qiu等[17]采用水-Bu OH-MTBE-ACN-TFA(5∶4∶1∶1∶0.001)为两相溶剂系统从紫薯中成功分离出3种酰基化花色苷单体,质量分数均不小于95%。除了上述提及的两相溶剂体系外,醋酸乙酯(EA)、BuOH、水和TFA组成的溶剂体系也可以用于分离花色苷单体。2013年,Li等[22]采用Bu OH-MTBE-ACN-0.1%TFA(0.715∶1.0∶0.134∶1.592)和BuOH-EA-ACN-0.1%TFA(1.348∶1.0∶0.605∶2.156)2个溶剂体系联用,成功地从木瓜花瓣中分离出飞燕草素3-O-葡萄糖苷等6种花色苷单体。
| 图表编号 | XD00200688600 严禁用于非法目的 |
|---|---|
| 绘制时间 | 2020.11.28 |
| 作者 | 孙恒勉、鲍虹蕾、童胜强 |
| 绘制单位 | 浙江工业大学药学院、浙江工业大学药学院、浙江工业大学药学院 |
| 更多格式 | 高清、无水印(增值服务) |