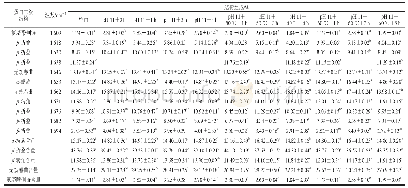
《表3 p H值偏移处理对油莎豆蛋白二级结构的影响》
注:结果以±s表示(n=3);同列不同字母表示差异显著(P<0.05)。
由表3可知,随p H值增加,二级结构中β-折叠相对含量显著降低,α-螺旋相对含量显著增加,β-转角和无规卷曲相对含量也略有增加。多肽链上羰基和氨基之间的氢键是维持α-螺旋稳定的主要作用力[21]。油莎豆蛋白等电点为4.5,在中性条件下蛋白带负电荷,在酸性条件下α-螺旋相对含量低可能是因为蛋白分子间电荷发生中和反应,产生静电作用,影响氢键的稳定性[22]。说明静电作用和氢键稳定性都会影响α-螺旋含量[23]。β-折叠含量还与蛋白质的疏水相互作用有关,其含量降低表明分子内部的疏水性位点暴露,疏水性增强[24],因此在p H?6~9的范围内,油莎豆蛋白β-折叠相对含量降低,表面疏水性增加。随着p H值增加,β-转角相对含量也略有增加,也可以说明p H值增加使蛋白质结构更加舒展[25]。
| 图表编号 | XD00195487100 严禁用于非法目的 |
|---|---|
| 绘制时间 | 2020.11.25 |
| 作者 | 王琳、周国卫、于志超、孟洛冰、王玉莹、张安琪、王喜波、江连洲 |
| 绘制单位 | 东北农业大学食品学院、东北农业大学食品学院、东北农业大学食品学院、东北农业大学食品学院、东北农业大学食品学院、东北农业大学食品学院、东北农业大学食品学院、东北农业大学食品学院 |
| 更多格式 | 高清、无水印(增值服务) |
 提示:宽带有限、当前游客访问压缩模式
提示:宽带有限、当前游客访问压缩模式