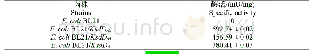
《表2 重组酶ArAsd的动力学参数》
 提示:宽带有限、当前游客访问压缩模式
提示:宽带有限、当前游客访问压缩模式
本系列图表出处文件名:随高清版一同展现
《不动杆菌来源L-天冬氨酸-β-脱羧酶的表达与酶学性质分析》
重组纯酶ArAsd在常规测定条件下(37℃,pH4.5)比酶活力为753 U/mg,较已有报道Pseudomonas sp.[7]来源的Asd比酶活力高1.7倍,较Alcaligenes faecalis[8]来源的Asd酶高2.5倍。ArAsd酶动力学常数如表2所示,其Km值较Pseudomonassp.[7]来源Asd酶低8.57 mmol/L,较Alcaligenes faecalis[8]来源的Asd酶低5.95 mol/L,更易于与底物结合;同时,kcat值为Alcaligenes faecalis[8]来源的Asd酶的2倍,表明其分子活力更高。较高的kcat/Km说明ArAsd具有更高的催化效率。
| 图表编号 | XD00170975200 严禁用于非法目的 |
|---|---|
| 绘制时间 | 2020.06.25 |
| 作者 | 于佳印、赵庭、刘中美、周丽、周哲敏 |
| 绘制单位 | 江南大学生物工程学院、江南大学生物工程学院、江南大学生物工程学院、江南大学生物工程学院、江南大学生物工程学院 |
| 更多格式 | 高清、无水印(增值服务) |