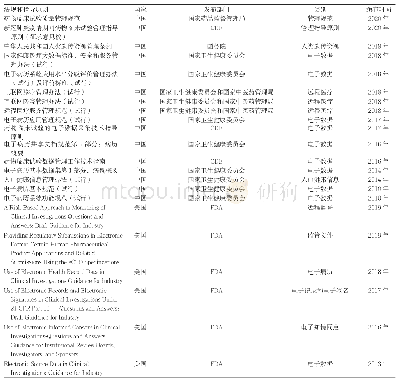
《表3 国内外不同监管机构颁布的致癌试验指导原则》
从1995年开始,ICH、FDA等机构发布了多项与致癌试验相关的指导原则,分别从致癌试验开展的必要性、致癌性试验设计、致癌性试验的数据统计学分析、考虑要点、剂量选择等方面给予规范和阐述,如表3所示[1,20-28]。2010年,我国原国家食品药品监督管理局(State Food and Drug Administration,SFDA)发布了《药物致癌试验必要性的技术指导原则》[27],但比国外指导原则发布晚了近5年,可见我国在此领域发展较国外晚,尚有大量工作需要推进。
| 图表编号 | XD0083316100 严禁用于非法目的 |
|---|---|
| 绘制时间 | 2019.08.20 |
| 作者 | 杨艳伟、刘甦苏、吕建军、王三龙、张素才、柳全明、范昌发 |
| 绘制单位 | 中国食品药品检定研究院国家药物安全评价监测中心药物非临床安全评价研究北京市重点实验室、中国食品药品检定研究院实验动物资源研究所、中国食品药品检定研究院国家药物安全评价监测中心药物非临床安全评价研究北京市重点实验室、中国食品药品检定研究院国家药物安全评价监测中心药物非临床安全评价研究北京市重点实验室、北京昭衍新药研究中心股份有限公司、中国食品药品检定研究院实验动物资源研究所、中国食品药品检定研究院实验动物资源研究所 |
| 更多格式 | 高清、无水印(增值服务) |
 提示:宽带有限、当前游客访问压缩模式
提示:宽带有限、当前游客访问压缩模式