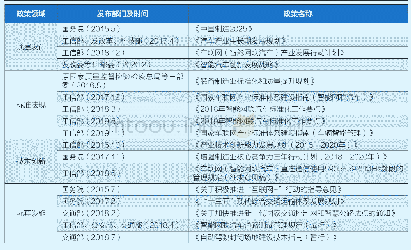
《表1 国内外智能化临床研究的相关法规和指导原则》
CDE:国家药品监督管理局药品审评中心,FDA:美国食品和药物管理局,EMA:欧洲药品管理局,MHRA:英国药品和健康产品管理局,DIA:药物信息协会,ICH:人用药品注册技术要求国际协调会,SCDM:临床数据管理学会
近年来,欧美等发达国家陆续发布了针对智能化、电子化临床研究的基本原则与行业指南;同时我国也颁布了一系列临床电子数据管理相关的指南性文件。随着智能化临床研究的深入实践,相关法规将不断完善,为行业提供指导。具体国内外相关法规文件及指导原则见表1。
| 图表编号 | XD00176156500 严禁用于非法目的 |
|---|---|
| 绘制时间 | 2020.06.25 |
| 作者 | 曹国英、付海军、何为、蒋薇薇、李华芳、李进、林峰、陆菁、马延、覃龙、阮秀芳、沈一峰、宋毅、王方敏、伍蓉、徐瑛、元唯安、张菁、张瑞雯、张晓敏 |
| 绘制单位 | 上海市药学会 |
| 更多格式 | 高清、无水印(增值服务) |
 提示:宽带有限、当前游客访问压缩模式
提示:宽带有限、当前游客访问压缩模式