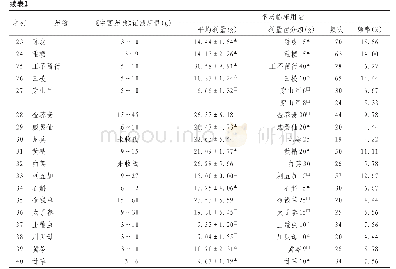
《表3 欧洲药典与中国药典关于aP毒性和效力质量标准的规定》
由于百日咳疫苗的复杂性,加之药品管理理念不同,不同国家和地区的质量标准并不一致。例如,美国食品药品管理局(FDA)只有指导意见而没有具体检测方法和标准的要求。欧洲药典和中国药典中aP关键检测项目的质量标准也有很大差异[27-28](表3)。由于百日咳疫苗检定主要依靠动物实验,动物不同品系乃至相同品系个体之间的差异也影响质量标准制定和检测结果。一些复杂操作如脑腔攻击也存在不同操作者的差异。随着疫苗质量提升,特别是抗原成分含量明确,百日咳疫苗的检定也发展出特异性更强、减少或不使用动物的检定方法。在临床上通常以体液免疫水平进行评价,即基础免疫完成后有效抗原(PT、FHA和PRN等)的抗体酶标单位呈4倍以上增长作为有效判定标准,但这实际忽略了一部分细胞免疫的评价。这可能是出现上市无细胞疫苗效力持久性不佳的原因之一。
| 图表编号 | XD0082520900 严禁用于非法目的 |
|---|---|
| 绘制时间 | 2019.06.26 |
| 作者 | 骆鹏、马霄 |
| 绘制单位 | 中国食品药品检定研究院国家卫生健康委员会生物技术产品检定方法及其标准化重点实验室、中国食品药品检定研究院国家卫生健康委员会生物技术产品检定方法及其标准化重点实验室 |
| 更多格式 | 高清、无水印(增值服务) |
 提示:宽带有限、当前游客访问压缩模式
提示:宽带有限、当前游客访问压缩模式
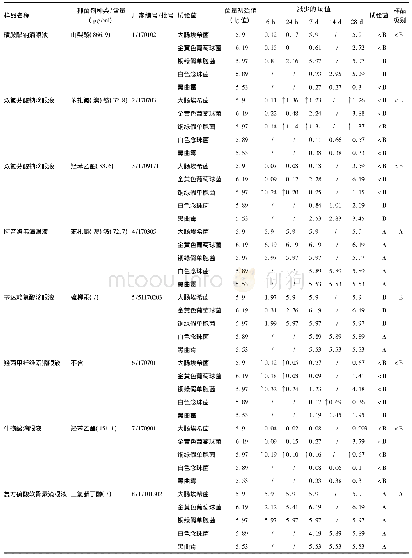
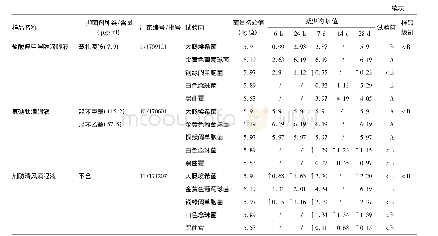
![表3《美国药典》与《欧洲药典》中关于禁用有机磷和有机氯农药残留限量标准[5-6]](http://bookimg.mtoou.info/tubiao/gif/NYXD202005013_01200.gif)
![表3《美国药典》与《欧洲药典》中关于禁用有机磷和有机氯农药残留限量标准[5-6]](http://bookimg.mtoou.info/tubiao/gif/NYXD202005013_01201.gif)