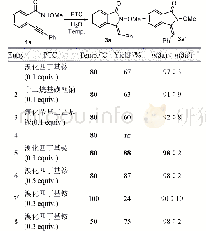
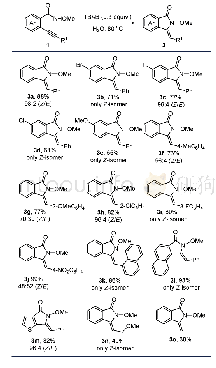
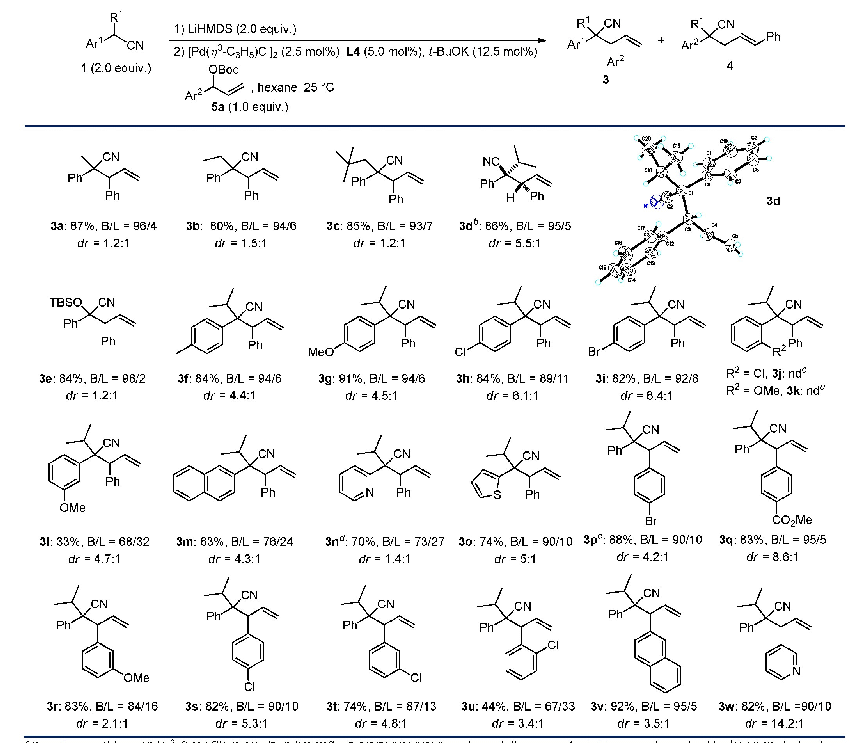
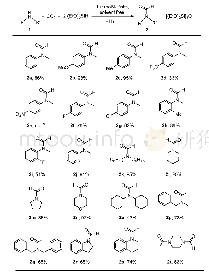
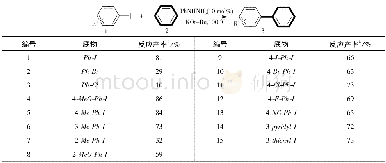
《表2 杂环的底物拓展a:富电子杂环芳烃与酮酯的自由基脱氢偶联反应》
a Reaction condition:heteroarene(1 equiv.,0.2 mmol),TBPA(3 equiv.,0.6 mmol),ester/ketone as solvent(6 m L),130℃,1 h,sealed tube;furan(1 equiv.,0.2mmol),CuI(10%mol,0.02 mmol),ketones as solvent(5 mL),N2,115℃,12 h,sealed tube,unless otherwise noted.b Isola
在最佳反应条件下,考察了一系列富电子杂环底物,均以中等到良好的产率得到目标产物(表2).芳环上不同甲基取代的N-甲基吲哚以中等产率得到相应的C(2)官能化产物(2~5).吲哚中C(5)位取代的卤素如氟、氯、溴和碘在该体系中都能稳定存在,以中等产率发生单一位置的CDC反应(6~9).紧接着考察了电子效应对该反应的影响.富电子的取代基团如甲氧基和苄氧基的吲哚也能够顺利进行反应(10,11).令人高兴的是C(3)位吸电子基团如羧基、乙酰基和酯基取代的吲哚分别以76%,74%和73%的良好产率得到目标产物(12~14).一些敏感活泼的官能团如羟基和烷基溴在该条件下均能耐受(15~17).吡咯类的含氮杂环同样能够进行该类型反应(19~22),其中值得注意的是,N-甲基吡咯得到了单取代和双取代的混合产物.不同取代的呋喃类底物在相应的反应条件下得到C(2)位取代的相应产物(23~26).有意思的是,底物C(3)位取代的呋喃反应位点发生在C(2)位,而不是位阻效应更小的C(5)位.这可能跟反应生成更稳定的苄位自由基中间体密切相关(24).接下来,考察了一系列低沸点的酯和酮与杂环芳烃的反应情况.乙酸甲酯、乙酸乙酯和丙酸乙酯与吲哚的反应高选择性地发生在羰基α-C(sp3)—H位置(27~32).杂环与各种酮交叉脱氢偶联反应顺利进行(33~38).不对称的酮均以高选择性发生在单一位点,这表明反应中自由基中间体的稳定性起到了决定性的作用.
| 图表编号 | XD003178400 严禁用于非法目的 |
|---|---|
| 绘制时间 | 2019.09.15 |
| 作者 | 肖莹霞、柳忠全 |
| 绘制单位 | 兰州大学化学化工学院功能有机分子化学国家重点实验室、兰州大学化学化工学院功能有机分子化学国家重点实验室、南京中医药大学药学院 |
| 更多格式 | 高清、无水印(增值服务) |
 提示:宽带有限、当前游客访问压缩模式
提示:宽带有限、当前游客访问压缩模式