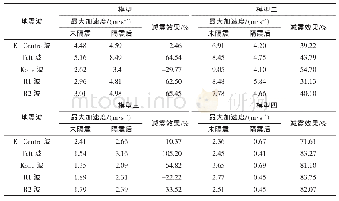
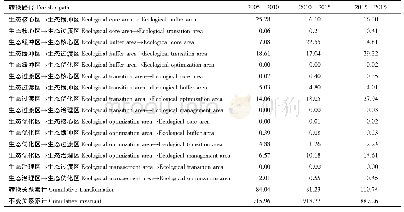
《表4 美国5种加速审评路径》
注:(1) FDASIA:《FDA安全性和创新法案》(Food and Drug Administration Safety and Innovation Act);(2) IND:研究性新药(Investigational New Drug)。
美国在不同历史时期设置5种审评路径,孤儿药依据是否符合特定条件可考虑进入优先审评[21](Priority Review)、加速审评[22-23](Accelerated Approval)、快速通道[24-25](Fast Track)程序,也可同时获得突破性疗法[26](Breakthrough Therapy)和再生医学先进疗法[27](Regenerative Medicine Advanced Therapy,RMAT)认定并获得审评激励(表4)。
| 图表编号 | XD00216370500 严禁用于非法目的 |
|---|---|
| 绘制时间 | 2020.12.20 |
| 作者 | 李壮琪、许文秀、杨殿政、卫付茜、杨悦 |
| 绘制单位 | 沈阳药科大学工商管理学院、国际食品药品政策与法律研究中心、沈阳药科大学工商管理学院、国际食品药品政策与法律研究中心、沈阳药科大学工商管理学院、国际食品药品政策与法律研究中心、沈阳药科大学工商管理学院、国际食品药品政策与法律研究中心、沈阳药科大学工商管理学院、国际食品药品政策与法律研究中心、清华大学药学院 |
| 更多格式 | 高清、无水印(增值服务) |
 提示:宽带有限、当前游客访问压缩模式
提示:宽带有限、当前游客访问压缩模式