《表1 美国生物类似药上市批准情况》
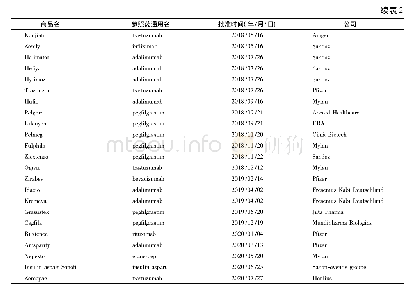
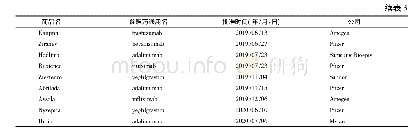
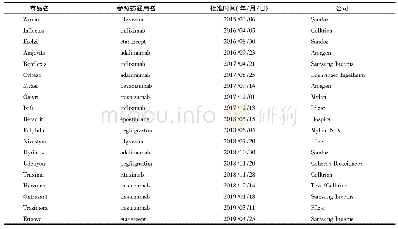
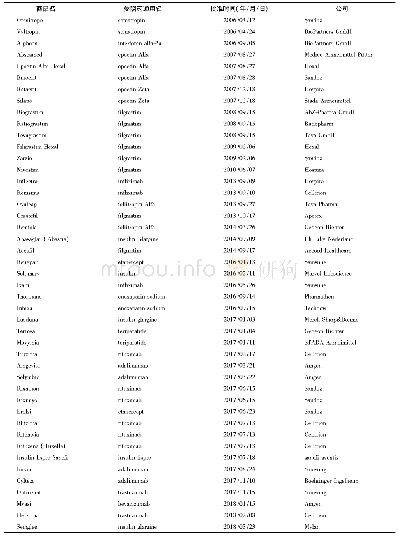
2015年3月—2018年6月,FDA已批准了根据8种不同参照药开发的11个生物类似药[16],具体为:非格司亭生物类似物1个,阿达木单抗生物类似物2个,英夫利昔单抗生物类似物3个,贝伐珠单抗生物类似物1个,曲妥珠单抗生物类似物1个,依那西普生物类似物1个,阿法依泊汀生物类似药1个,培非司亭生物类似药1个,其中单抗药物4个。但是,鉴于相关法规的不足,美国已批准上市的生物类似药在临床的应用和综合效益尚未实现预期的目标。虽然如此,多家研究公司预测,未来美国生物类似药的使用将超过欧盟。美国批准上市的生物类似药见表1。
| 图表编号 | XD0032350000 严禁用于非法目的 |
|---|---|
| 绘制时间 | 2019.04.28 |
| 作者 | 李光慧、林涛、王海辉、杨建红 |
| 绘制单位 | 安进生物技术咨询(上海)有限公司、安进生物技术咨询(上海)有限公司、辉瑞投资有限公司、沈阳药科大学亦弘商学院 |
| 更多格式 | 高清、无水印(增值服务) |
 提示:宽带有限、当前游客访问压缩模式
提示:宽带有限、当前游客访问压缩模式

![表2 中国已获批上市的8款生物类似药[4]](http://bookimg.mtoou.info/tubiao/gif/SYZZ202101004_02200.gif)