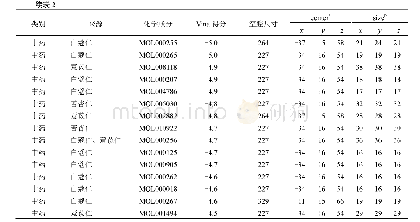
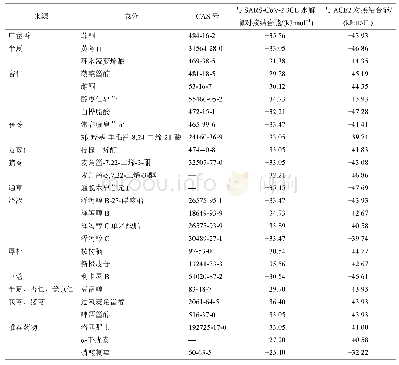
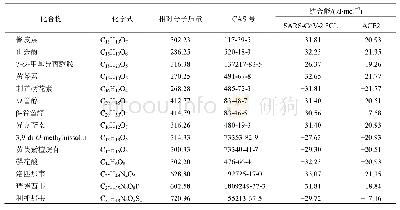
《表1 含不同类别Michael受体化合物对SARS-CoV 3CL R188I蛋白酶抑制活性的比较》
a) n.i.表示没有抑制活性.
Yang等[62]在前文介绍的化合物7的基础上,为了提高化合物的细胞活性,将P2位更换为环己基丙氨酸,同时为了避免C端反应基团被酯酶水解,将共价反应头由不饱和酯换为醛类(反应机理见图5(b)),得到化合物8 (图7).化合物8的抑制常数Ki值为53 nM,抗SARS病毒的半数有效浓度(EC50)值为0.6μM.Akaji等[63]发现,成熟的SARS-CoV 3CL蛋白酶在Arg188/Gln189处易被降解,而将188位的Arg突变成Ile后蛋白稳定性增强,并且催化活性提高了接近106倍.随后,该团队试图采用R188I突变蛋白去发现活性更强的抑制剂.根据天然底物的序列,设计并合成了C-末端为醛类的五肽抑制剂(化合物9),其抑制SARS-CoV 3CL蛋白酶R188I的半数抑制浓度(IC50)值为37μM.采用与化合物9相同的氨基酸序列,将C端更换为不可逆的Michael受体,得到化合物10,以及类似物11和12,从表1可以看出,醛类抑制剂比不饱和酯类抑制剂对R188I突变蛋白具有更强的抑制活性[64].以8为先导化合物,首先考察不同类型的P1取代基对活性的贡献,得到化合物13,IC50为5.7μM.根据SARS-CoV 3CL蛋白酶R188I蛋白与化合物8的共晶结构,对P2位进行结构优化,发现P2位为环己基时活性最佳,IC50为65 nM (化合物14).为了解决肽链易被酶解以及共价结合的毒性问题,该团队在前期研究的醛类抑制剂基础上,引入新型骨架来代替肽键和采用更安全的反应头基团替换醛基.先后设计了氢化异喹啉骨架(化合物15)[65]和八氢异色烯骨架(化合物16)拟肽抑制剂,对化合物15进一步改造得到了亲水性增加的化合物17和硫缩醛反应头衍生物18,遗憾的是,这些化合物的酶活抑制能力一般,有待进一步优化.2017年,Kumar等[66]通过化学改造得到了一系列可以同时抑制SARS-CoV 3CL蛋白酶和MERS-CoV 3CL蛋白酶的醛类抑制剂,其中有3个类似物(化合物19、20和21)抗MERS-CoV的活性在微摩尔浓度.
| 图表编号 | XD00222275200 严禁用于非法目的 |
|---|---|
| 绘制时间 | 2020.10.20 |
| 作者 | 李春梅、孙琦、陆阳彬、刘莹、来鲁华 |
| 绘制单位 | 北京大学化学与分子工程学院北京分子科学国家研究中心、北京大学前沿交叉学科研究院定量生物学中心、北京大学化学与分子工程学院北京分子科学国家研究中心、北京大学化学与分子工程学院北京分子科学国家研究中心、北京大学化学与分子工程学院北京分子科学国家研究中心、北京大学前沿交叉学科研究院定量生物学中心、北京大学化学与分子工程学院北京分子科学国家研究中心、北京大学前沿交叉学科研究院定量生物学中心、北京大学-清华大学生命科学联合中心 |
| 更多格式 | 高清、无水印(增值服务) |
 提示:宽带有限、当前游客访问压缩模式
提示:宽带有限、当前游客访问压缩模式