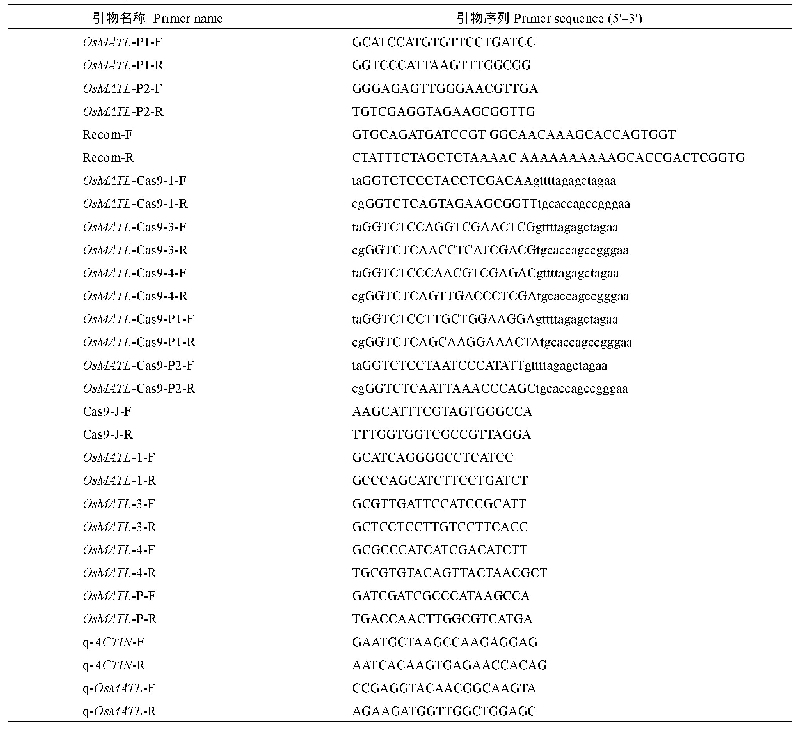
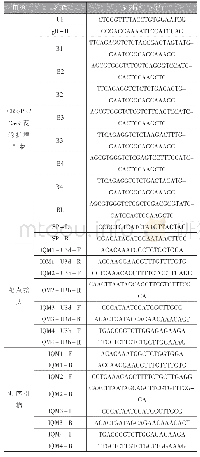
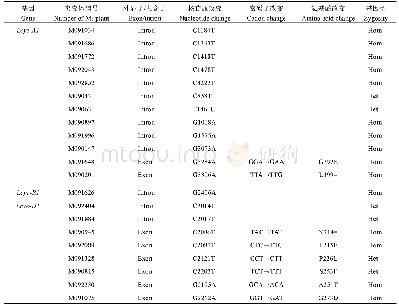
《表1 利用TILLING技术筛选Lcye突变体的引物信息》
EMS突变库筛选参照Till等[19]方法,具体步骤如下:(1)突变体DNA池构建:应用CTAB法[20]分别提取每个M2突变体植株的基因组DNA,将其存放于96孔板中。利用NanoDrop-2000超微量分光光度仪(thermo scientific)测定DNA的浓度和质量。按8个样品一组将DNA进行等量混合,构建8倍DNA混合池,4℃保存备用。(2)Lcye特异性引物设计:基于小麦Lcye同源基因序列差异,设计A、B和D基因组特异性引物。利用中国春缺体-四体材料及PCR产物测序方法,进行引物基因组特异性验证;应用CODDLE(codons optimized to discover deleterious lesions,http://www.proweb.org/coddle/)软件分析扩增区域是否对基因功能起重要作用。最终4对Lcye特异性引物,用于突变体筛选(表1)。(3)PCR扩增与异源双链生成:以DNA混合池为模板进行PCR扩增,反应体系:DNA 50 ng,PreMix 7.5μL,10μmol L?1上、下游引物各1μL,ddH2O补足至15μL;反应程序:首先95℃变性5 min;然后95℃变性30 s,退火温度从66℃开始,每个循环降低0.3℃,退火45 s,72℃延伸1.5 min,重复35个循环;72℃延伸10 min;然后99℃10 min,85℃1 min,退火温度从85℃开始,每个循环降低0.5℃,退火时间30 s,共99个循环;最后16℃保温备用。如果DNA混合池样本目标片段中含有突变位点,扩增产物经过反复变性、复性将形成野生型和突变体扩增片段的异源双链(即含有错配碱基)。(4)CEL I酶切:用特异性识别并切割错配碱基的核酸内切酶CEL I剪切异源双链核酸分子。酶切反应体系:10×消化缓冲液2μL,CEL I 1μL,异源双链DNA 15μL,ddH2O补足至20μL。45℃反应20 min,随后加入EDTA(0.25 mol L–1)5μL终止酶切反应。(5)非变性聚丙烯酰胺凝胶电泳检测:利用非变性聚丙烯酰胺凝胶电泳技术检测CEL I酶切片段,筛选获得含有突变位点的阳性DNA混合池。对阳性DNA混合池中的每个样本DNA逐一与野生型DNA进行等量混合,重复上述步骤,筛选获得阳性突变体单株。(6)突变样本克隆测序:对突变个体PCR产物进行克隆测序,鉴定突变类型和位置。
| 图表编号 | XD00156931300 严禁用于非法目的 |
|---|---|
| 绘制时间 | 2020.10.12 |
| 作者 | 翟胜男、郭军、刘成、李豪圣、宋健民、刘爱峰、曹新有、程敦公、李法计、何中虎、夏先春、刘建军 |
| 绘制单位 | 山东省农业科学院作物研究所、山东省农业科学院作物研究所、山东省农业科学院作物研究所、山东省农业科学院作物研究所、山东省农业科学院作物研究所、山东省农业科学院作物研究所、山东省农业科学院作物研究所、山东省农业科学院作物研究所、山东省农业科学院作物研究所、中国农业科学院作物科学研究所、中国农业科学院作物科学研究所、山东省农业科学院作物研究所 |
| 更多格式 | 高清、无水印(增值服务) |
 提示:宽带有限、当前游客访问压缩模式
提示:宽带有限、当前游客访问压缩模式