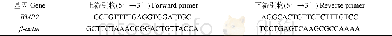《表2 Apo B、β-actin特异性引物序列》
三组受试者空腹12~14 h后采静脉血5 ml,加入肝素抗凝,1 000/min离心5 min,血浆置-80℃保存,逆转录-聚合酶链式反应(RT-PCR)和琼脂糖凝胶电泳法检测血浆Apo B含量[2]。培养HepG2(肝癌细胞系)细胞,对一部分细胞进行细胞转染,加入pHBV1.3质粒,未转染过的细胞标为HepG2.1,转染过的细胞标为HepG2.2,将细胞放置于加入了转染液的细胞培养基中,在CO2培养箱中继续培养。然后进行RT-PCR和琼脂糖凝胶电泳法检测:对转染和未转染的两种细胞用TRIzolR试剂提取细胞总RNA,经DNA酶处理后取1μg用反转录酶合成cDNA,然后对ApoB基因的RT-PCR检测引物进行检测,同时以β-actin作为内参照进行平行扩增(ApoB、β-actin特异性引物序列见表2),采用软件Primer Premier5.0进行引物设计,扩增产物采用琼脂糖凝胶电泳进行检测[2]。对转染与未转染pH-BV1.3质粒HepG2细胞中AopB mRNA的表达进行比较,以观察HBV对AopB表达的影响。
| 图表编号 | XD0047134100 严禁用于非法目的 |
|---|---|
| 绘制时间 | 2019.01.20 |
| 作者 | 卢燕辉、徐成润、卢秋燕、吴贺华 |
| 绘制单位 | 解放军第175医院感染科、解放军第175医院感染科、解放军第175医院感染科、解放军第175医院感染科 |
| 更多格式 | 高清、无水印(增值服务) |
 提示:宽带有限、当前游客访问压缩模式
提示:宽带有限、当前游客访问压缩模式