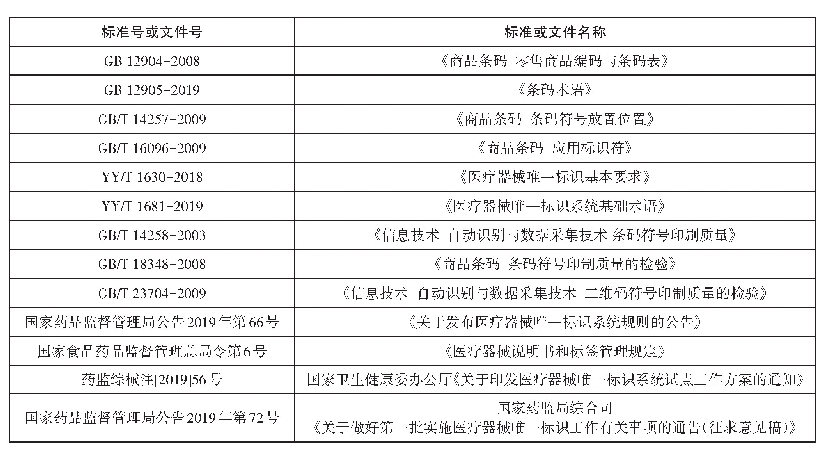
《表1 IMDRF文件和部分国家UDI法规中UDI-PI相关内容》
国际医疗器械监管机构论坛(international medical device regulators forum,IMDRF)的主要目的是促进全球医疗器械监管法规的协调和融合,目前已经发布了2份关于UDI的指南文件,是各国家和地区制定UDI法规的重要参考,除我国外,美国、欧盟委员会也已经发布UDI系统的相关法规文件,表1梳理了IMDRF指南和各国家和地区法规中关于UDI-PI的相关内容。
| 图表编号 | XD00218808500 严禁用于非法目的 |
|---|---|
| 绘制时间 | 2021.01.30 |
| 作者 | 易力、荆敏琪、余新华 |
| 绘制单位 | 中国食品药品检定研究院医疗器械标准管理研究所、中国食品药品检定研究院医疗器械标准管理研究所、中国食品药品检定研究院医疗器械标准管理研究所 |
| 更多格式 | 高清、无水印(增值服务) |
 提示:宽带有限、当前游客访问压缩模式
提示:宽带有限、当前游客访问压缩模式