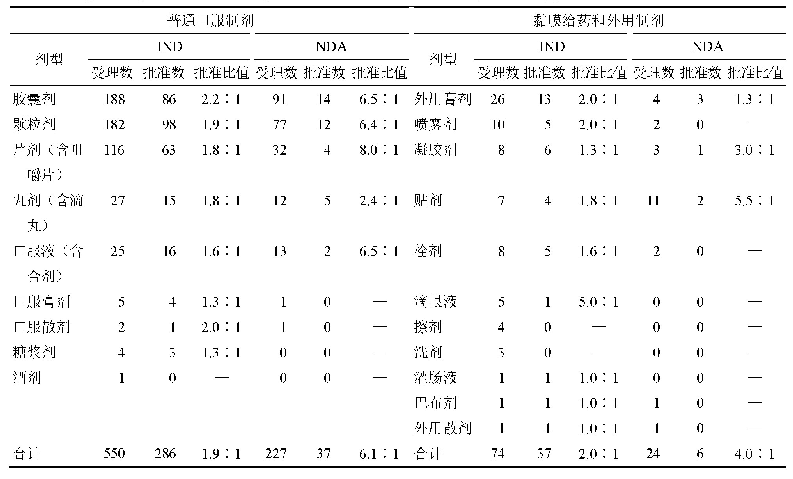
《表4 2017—2019年CDE批准的中药新药申请相关剂型情况》
 提示:宽带有限、当前游客访问压缩模式
提示:宽带有限、当前游客访问压缩模式
本系列图表出处文件名:随高清版一同展现
《2007—2019年国内中药新药注册的审批情况分析》
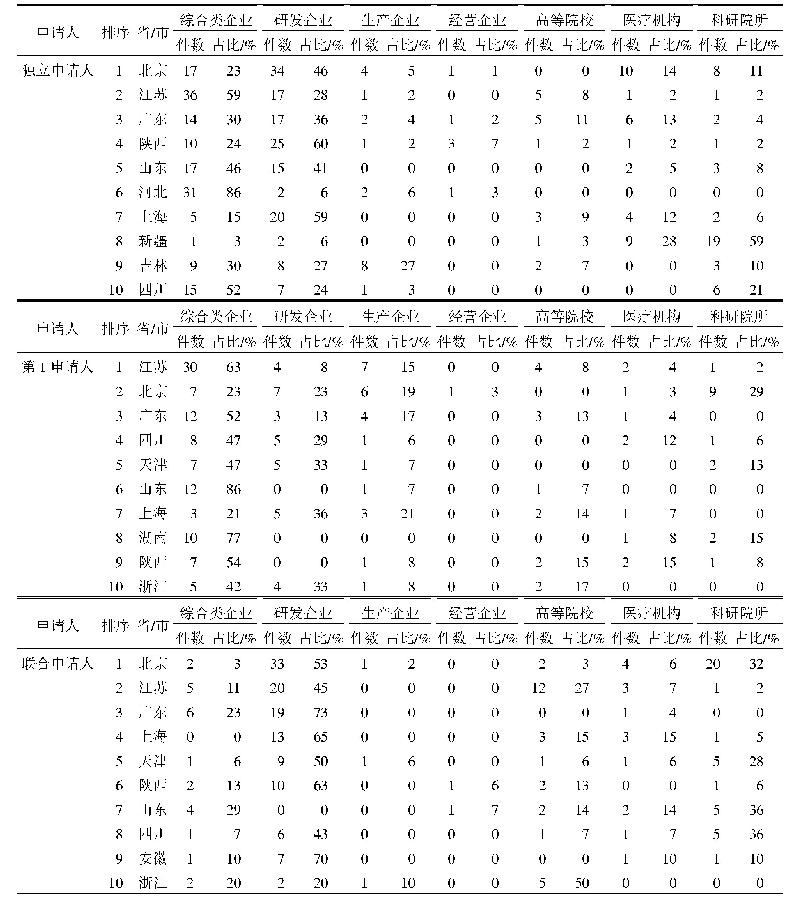
2007—2019年CDE受理的中药新药申请中,涉及制剂的申请共有897件,主要为普通口服制剂(87%)、黏膜给药和外用制剂(11%)、注射剂(2%)这3大类,且细分为IND和NDA后仍呈类似分布。就具体剂型的构成而言(表4),在普通口服制剂申请中,总体申请及细分为IND和NDA后,均以胶囊剂、颗粒剂和片剂占据绝大部分比例,合计约88%,另有约10%为口服液和丸剂,约2%为糖浆剂、散剂等。在黏膜给药和外用制剂申请中,IND和NDA则表现出了不同的构成特点;IND涉及最多的为外用膏剂(33%),其余依次是喷雾剂(14%)、凝胶剂(11%)、栓剂(11%)、贴剂(10%)、滴眼液(7%)、擦剂(6%)等;而NDA制剂申请以贴剂(46%)最为多见,其余主要还涉及外用膏剂(17%)、凝胶剂(13%)、喷雾剂(8%)和栓剂(8%)等。注射剂共涉及22件,这类剂型自2011年起少有涉及,近3年未见申请。
| 图表编号 | XD00215755100 严禁用于非法目的 |
|---|---|
| 绘制时间 | 2021.02.12 |
| 作者 | 瞿礼萍、陈杨、王筱竺、邹文俊、刘毅 |
| 绘制单位 | 成都中医药大学药学院、成都中医药大学药学院、成都中医药大学药学院、成都中医药大学药学院、成都中医药大学药学院 |
| 更多格式 | 高清、无水印(增值服务) |
![表3 2016-2019年美国拓展性同情用药申请与批准量[12]](http://bookimg.mtoou.info/tubiao/gif/ZGYS202012010_04600.gif)