《表4 高脂日粮诱导的动物胰岛素抵抗模型》
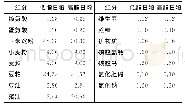
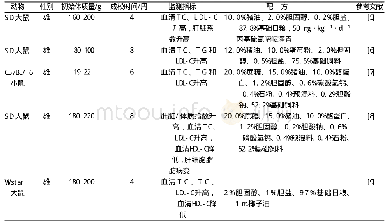
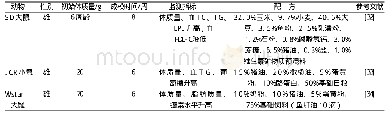
研究指出,受体部位对体内外胰岛素的敏感性下降是直接造成胰岛素抵抗的核心机制。临床研究认为,胰岛素抵抗容易引起糖尿病和动脉粥样疾病的发生率升高,同时与肥胖和心血管等疾病有密切联系[23]。诱导该模型的饲料以基础料+胆固醇+猪油+糖为主,并可通过增加糖分含量缩短模型建立周期[24-26](表4);高脂饲料在制备环节中,蛋白质、脂肪与碳水化合物充分混合加热,导致高级糖化产物(advanced glycation end-products,AGEs)的形成,更加有利于该疾病模型的建立[27]。研究认为,胰岛素抵抗的发生主要是由于长期血液中高水平的游离脂肪酸(free fat acid,FFA)引起内质网应激、自由基侵袭、细胞凋亡和炎性反应,使正常的胰岛素信号转导不能实现,引起胰岛素抵抗发生;其中,信号途径c-Jun氨基末端激酶(c-Jun N-terminal kinase,JNK)和核因子-κB激酶抑制剂/核转录因子-κB(inhibitor of nuclear factor kappa-B kinase/nuclear transcription factor-κB,IKK/NF-κB)之间交互作用造成的损伤是FFA诱发胰岛素抵抗的主要诱因[28]。血液FFA可使胰岛素受体的结构因发生磷酸化而改变,影响正常的酪氨酸磷酸化和磷脂酰肌醇-3激酶(phosphoinositide 3-kinases,PI3Ks)活性,胰岛素信号通路受阻。此外,活化后的丝氨酸/苏氨酸激酶(serine/threonine kinases,AKT)可以通过调节包括糖原合成酶激酶-3β(glycogen synthase kinase-3β,GSK-3β)在内的一系列下游分子而增加糖原生成,同时叉头框转录因子O亚族1(forkhead box O1,Fox O1)磷酸化后导致自身功能异常,影响磷酸烯醇式丙酮酸激酶(phosphoenol-pyruvatecarboxy-kinase 1,PCK1)和葡萄糖-6-磷酸酶(glucose 6 phosphatase,G6Pase)在体内的糖异生作用,增加胰岛素抵抗的发生风险[29]。
| 图表编号 | XD00208344300 严禁用于非法目的 |
|---|---|
| 绘制时间 | 2021.02.25 |
| 作者 | 罗建波、李军晖、王海江、周小玉、曾涛、周佳、朱献军 |
| 绘制单位 | 四川省医学科学院.四川省人民医院实验动物研究所、四川省医学科学院.四川省人民医院实验动物研究所、四川省医学科学院.四川省人民医院实验动物研究所、四川省医学科学院.四川省人民医院实验动物研究所、四川省医学科学院.四川省人民医院实验动物研究所、四川省医学科学院.四川省人民医院实验动物研究所、四川省医学科学院.四川省人民医院人类疾病基因研究四川省重点实验室 |
| 更多格式 | 高清、无水印(增值服务) |
 提示:宽带有限、当前游客访问压缩模式
提示:宽带有限、当前游客访问压缩模式