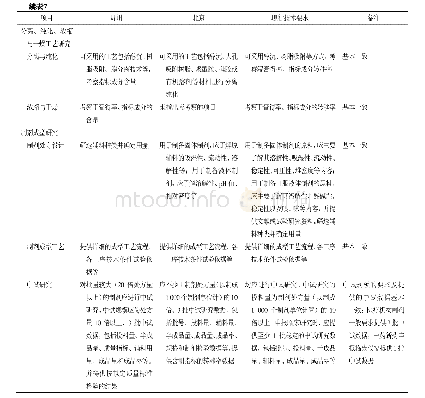
《表3 简化注册资料要求比较》
 提示:宽带有限、当前游客访问压缩模式
提示:宽带有限、当前游客访问压缩模式
本系列图表出处文件名:随高清版一同展现
《欧盟传统草药注册制度对我国经典名方简化注册监管体系的启示》
我国对于符合简化注册审批要求的经典名方注册申报资料同样进行减免,申请者只需提交综述资料、药学资料以及非临床研究资料,免除了临床试验研究资料及药效学研究资料。其中药学研究资料除药材、饮片炮制外,还应包括经典名方物质基准。但是由于我国尚未出台类似EUM或EULE的经典名方安全有效性评价官方文件,因此无法进一步减免注册资料。欧盟与我国简化注册资料要求比较见表3。
| 图表编号 | XD00201693600 严禁用于非法目的 |
|---|---|
| 绘制时间 | 2020.12.15 |
| 作者 | 葛文霞、钱欣诚、邵蓉 |
| 绘制单位 | 中国药科大学国家药物政策与医药产业经济研究中心、中国药科大学国家药物政策与医药产业经济研究中心、中国药科大学国家药物政策与医药产业经济研究中心 |
| 更多格式 | 高清、无水印(增值服务) |