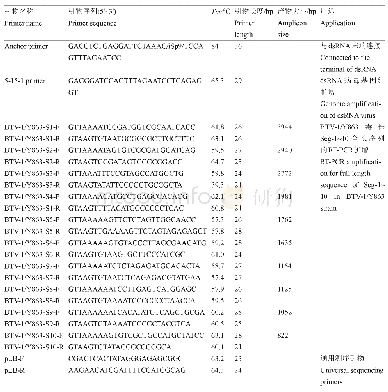
《表2 肠道病毒扩增测序引物》
 提示:宽带有限、当前游客访问压缩模式
提示:宽带有限、当前游客访问压缩模式
本系列图表出处文件名:随高清版一同展现
《2016-2018河北地区儿童病毒性脑炎流行特征调查》
选取肠道病毒样品,利用PCR扩增病毒VP1基因序列片段,引物设计参照GenBank和过往文献[11-12](表2)。采用A-OS/A-OAS引物对肠道病毒A群进行第一轮扩增;A-IS/A-IAS引物对肠道病毒A群进行第二轮扩增。同样,分别采用B-OS/B-OAS、B-IS/B-IAS引物分别对肠道病毒B群进行第一轮和第二轮扩增。第一轮反应液配置:2μl第一轮反应酶混合液,4μl Prime script burffer,4μl RNA模板,1μl PCR Forward Primer,1μl PCR Reverse Primer,ddH2O补足25μl。第一轮反应条件:50℃40min;94℃3min;94℃30s,55℃30s,72℃40s,循环35次;72℃8min。第二轮反应液配置:2.5μl Ex Taq DNA聚合酶,4μl Mg2+,4μl DNA模板,1μl PCR Forward Primer,1μl PCR Reverse Primer,ddH2O补足25μl。第二轮反应条件:94℃3min;94℃30s,55℃30s,72℃40s,循环35次;72℃8min。收集产物,将3μl产物放入电泳仪胶板中,采用含有嗅化乙锭(EB)的1%的琼脂糖凝胶,进行电泳(电压120V,30min)。凝胶采用Universal HoodⅡ凝胶成像分析系统成像,将扩增结果为阳性且清晰的样品进行测序。测序由生工生物工程(上海)股份有限公司完成,测序结果由Bio Edit进行矫正。将本次研究中获到的病毒VP1序列与NCBI的BLAST数据库中数据进行对比,若85%氨基酸与数据库中病毒具有同一性则认为是同一血清型。利用软件MEGA6.0对柯萨奇病毒B5绘制种系发生树,采用邻位相连法构建进化树。
| 图表编号 | XD00180013900 严禁用于非法目的 |
|---|---|
| 绘制时间 | 2019.12.30 |
| 作者 | 雷延龄、蒋秀芳、褚丽敏、赵倩 |
| 绘制单位 | 河北医科大学第二医院儿科、河北医科大学第一医院儿科 |
| 更多格式 | 高清、无水印(增值服务) |


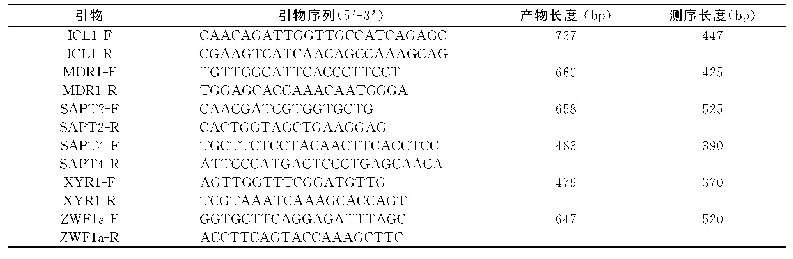
![表1 人细小病毒B19核酸检测试剂国家参考品PCR扩增及测序引物[6]](http://bookimg.mtoou.info/tubiao/gif/YXYQ202012003_01000.gif)