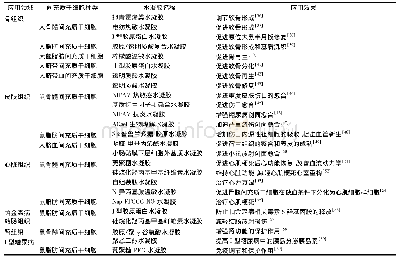
《表5 中美新药监管差异:间充质干细胞基础研究与临床转化的中美比较》
美国新药研发以政府服务、企业主导为特征,中国新药研发则较多以政府主导,企业介入不足。相比之下,美国医药消费市场份额大,其新药研发经费也较多。在新药审评程序、审评费用、新药医保方面均存在差异[13-14],具体见表5。具体在干细胞领域,美国的相关法律、法规和指南所涉及的问题相对全面[15],我国涉及干细胞药品(制剂)的法律法规仍旧亟待完善,包括《干细胞临床研究管理办法(试行)》等多处于试行阶段[16]。
| 图表编号 | XD00171440100 严禁用于非法目的 |
|---|---|
| 绘制时间 | 2020.04.01 |
| 作者 | 苑亚坤、刘广洋、刘拥军、谢亚芳、吴昊 |
| 绘制单位 | 中国科学院文献情报中心、中国科学院大学经济与管理学院、北京亦创生物技术产业研究院干细胞与再生医学研究所、北京贝来生物科技有限公司、北京亦创生物技术产业研究院干细胞与再生医学研究所、北京贝来生物科技有限公司、北京亦创生物技术产业研究院干细胞与再生医学研究所、北京贝来生物科技有限公司、中国科学院文献情报中心、中国科学院大学经济与管理学院 |
| 更多格式 | 高清、无水印(增值服务) |
 提示:宽带有限、当前游客访问压缩模式
提示:宽带有限、当前游客访问压缩模式