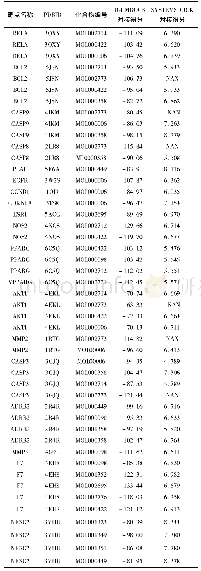
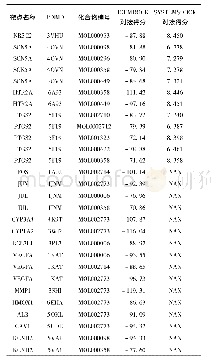
《表1 ETC与Tfs相互作用的结合参数》
以lg[(F0-F)/F]对lg[Q]作图(如图4所示),由曲线的截距和斜率即可求出Ka和n值,见表1。据表1数据可得,apo-Tf和holo-Tf与菁染料ETC的结合常数均可达到105(mol/L)-1,表明两种蛋白与ETC之间都存在较强的相互作用并形成了复合物。两种转铁蛋白与ETC的结合位点数约为1,说明ETC在转铁蛋白上主要有一个特异性结合位点。相比较而言,apo-Tf与ETC结合常数大于holo-Tf与ETC,说明apo-Tf具有更强的结合能力。其主要原因猜测是两种转铁蛋白本身的构象不同:apo-Tf未与铁离子结合而处于开放状态,holo-Tf与两个铁离子结合而处于闭合状态。ETC很可能通过非共价键作用,插入到apo-Tf的开放区域,因此apo-Tf可以有更多的氨基酸残基与ETC相互作用。对于holo-Tf,本身为闭合构象,所以ETC只能和其表面的氨基酸残基相互作用。结果分析表明,开放状态下的apo-Tf与菁染料ETC的结合能力强于闭合状态下的holoTf与菁染料ETC的结合能力。
| 图表编号 | XD0088799800 严禁用于非法目的 |
|---|---|
| 绘制时间 | 2019.09.01 |
| 作者 | 张卜月、王伟、叶梅、王茜柳、张芳、付尧、张秀凤 |
| 绘制单位 | 华北理工大学化学工程学院、华北理工大学化学工程学院、华北理工大学化学工程学院、华北理工大学化学工程学院、华北理工大学化学工程学院、华北理工大学化学工程学院、华北理工大学化学工程学院 |
| 更多格式 | 高清、无水印(增值服务) |
 提示:宽带有限、当前游客访问压缩模式
提示:宽带有限、当前游客访问压缩模式