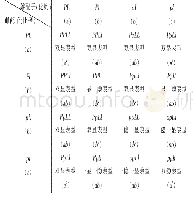
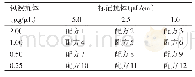
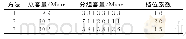《表1 棋盘法优化种毒条件的分组》
取出冻存的MDCK细胞,立即放置37~38℃温水浴中解冻,用10 m L完全培养基(含5%胎牛血清和4 nmol/L L-Glutamine的VP-SFM培养基)培养至T25细胞培养瓶,于37℃,5%CO2恒温细胞培养箱培养6~8 h;更换新鲜完全培养基,继续培养。稳定培养3代后,以3×106个/瓶接种至T75细胞培养瓶,加入17 m L完全培养基,于37℃,5%CO2恒温细胞培养箱培养24~30 h;用PBS洗涤2次,分别按MOI=0.1、0.01、0.001和0.000 1(用不含TPCK胰酶的病毒维持液将病毒进行稀释)接种H1N1(IVR-180)、H3N2(IVR-186)、BV(NYMC BX-69A)、BY(B/Phuket/3073/2013)疫苗株,加入17 m L病毒维持液(含终浓度分别为0.5、1、1.5、2、3和4μg/m L TPCK胰酶、1×青链霉素及4 nmol/L L-Glutamine的无血清VP-SFM培养基),其中H1N1(IVR-180)疫苗株病毒维持液的TPCK胰酶终浓度分别为0.5、1、1.5、2μg/m L,其他3株病毒维持液的TPCK胰酶终浓度分别为1、2、3和4μg/m L。棋盘法优化种毒条件分组见表1。每24 h取细胞培养上清液进行血凝滴度检测,至血凝滴度开始下降或细胞完全脱落;选取各疫苗株以血凝滴度评判为最适种毒条件(组间数据相同时,选取较低终浓度TPCK胰酶或较低MOI组为最佳)的组别进行病毒滴度检测,综合两项指标确定最佳收毒时间。
| 图表编号 | XD00209807700 严禁用于非法目的 |
|---|---|
| 绘制时间 | 2021.03.20 |
| 作者 | 李兴航、刘琛、张家友、闫璐瑶、韩天、刘博、李芳、宋颖丽、杨晓明 |
| 绘制单位 | 武汉生物制品研究所有限责任公司、国家联合疫苗工程技术研究中心、武汉生物制品研究所有限责任公司、国家联合疫苗工程技术研究中心、武汉生物制品研究所有限责任公司、国家联合疫苗工程技术研究中心、武汉生物制品研究所有限责任公司、国家联合疫苗工程技术研究中心、武汉生物制品研究所有限责任公司、国家联合疫苗工程技术研究中心、武汉生物制品研究所有限责任公司、国家联合疫苗工程技术研究中心、武汉生物制品研究所有限责任公司、国家联合疫苗工程技术研究中心、武汉生物制品研究所有限责任公司、国家联合疫苗工程技术研究中心、国家联合疫苗工 |
| 更多格式 | 高清、无水印(增值服务) |
 提示:宽带有限、当前游客访问压缩模式
提示:宽带有限、当前游客访问压缩模式