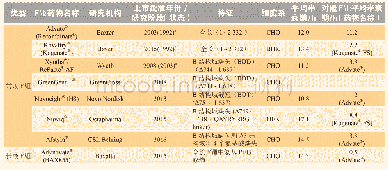
《表1 已批准的r FⅧ信息汇总》
为避免血液病毒的传播、不受血浆来源的限制,满足患者的用药需求,1992年,首款r FⅧ产品获批。根据工艺及制剂处方不同,r FⅧ划分为不同代次:第1代r FⅧ制品生产过程中添加了动物源血清,且制剂处方中添加了人血白蛋白作为稳定剂;第2代产品在生产过程中使用人源材料替代动物源材料(如牛血清),且制剂处方中用蔗糖或海藻糖作为稳定剂;第3代r FⅧ生产过程中使用全化学合成的培养基。除了生产工艺及制剂处方不同外,目前已批准的r FⅧ在序列上也有差异,包括含全长的FⅧ、B结构域缺失的r FⅧ。从生产使用的细胞基质看,目前已批准r FⅧ使用的表达细胞系包括CHO、BHK、HEK。另外,为延长r FⅧ的半衰期,目前还有r FⅧ-Fc、PEG化r FⅧ重组制品上市。国际上已批准的r FⅧ的相关信息见表1[6]。除上述类型的r FⅧ产品外,罗氏的双特异抗体Emicizumab能够模拟FⅧ分子,通过抑制天然抗凝血剂如抗凝血酶(antithrombin,AT)和组织因子途径抑制剂(tissue factor pathway inhibitor,TFPI)发挥作用,达到治疗血友病的效果,由于该产品与其他r FⅧ化学本质差异较大,本文不做重点讨论。
| 图表编号 | XD00208081200 严禁用于非法目的 |
|---|---|
| 绘制时间 | 2020.12.20 |
| 作者 | 邱晓 |
| 绘制单位 | 国家药品监督管理局药品审评中心 |
| 更多格式 | 高清、无水印(增值服务) |
 提示:宽带有限、当前游客访问压缩模式
提示:宽带有限、当前游客访问压缩模式