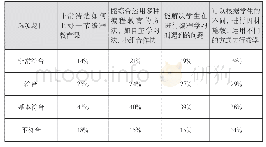
《表1 重编程因子和载体介导细胞体外重编程生成i OPCs及神经谱系细胞的策略》
 提示:宽带有限、当前游客访问压缩模式
提示:宽带有限、当前游客访问压缩模式
本系列图表出处文件名:随高清版一同展现
《介导诱导性少突胶质细胞祖细胞生成的重编程因子的研究进展》
Nano-HA:纳米羟基磷灰石;SHH:音猥因子;FGF:成纤维细胞生长因子;PDGF-AA:血小板源生长因子;m ESCs:小鼠胚胎干细胞;hi PSCs:人诱导性多能干细胞;MEFs:小鼠胚胎成纤维细胞;REFs:大鼠胚胎成纤维细胞;MLFs:小鼠肺成纤维细胞;h En SCs:人子宫内膜基质细胞;h NSCs:人神经干细胞;NSCs:
目前,体外重编程体细胞或多能干细胞生成i OPCs的策略主要采用逆转录病毒或慢病毒载体介导转录因子或mi RNA的表达(表1)。然而,外源性病毒载体和重编程因子在受体细胞基因组中的整合,使得生成的i OPCs具有潜在的致瘤性,从而限制了其在临床上的应用。非病毒载体因其相对安全且易于大规模生产而受到人们的广泛关注。常用的非病毒载体包括聚乙烯亚胺(polyethyleneimine,PEI)[59]、脂质体[60]和纳米颗粒[61]等,但是其转染效率相对较低。Arsianti等[62]发现,采用PEI包被的磁性氧化铁纳米颗粒转染乳仓鼠肾细胞(baby hamster syrian kidney cells,BHK21)时,PEI的氨基可以通过质子化作用使溶酶体的p H发生改变,从而导致溶酶体囊泡不稳定,避免了溶酶体对载体和外源基因的捕获,提高其转染效率。因此,寻求一种安全的体外重编程技术对于脱髓鞘疾病的再生治疗非常重要,小分子物质有望提供新的重编程策略。
| 图表编号 | XD0096091900 严禁用于非法目的 |
|---|---|
| 绘制时间 | 2019.08.01 |
| 作者 | 令文慧、王明玉、熊春霞、谢登峰、陈麒宇、褚新月、李云鑫、邱小燕、李跃民、肖雄 |
| 绘制单位 | 西南大学动物科技学院、西南大学动物科技学院、西南大学动物科技学院、西南大学动物科技学院、西南大学动物科技学院、西南大学动物科技学院、西南大学动物科技学院、西南大学动物科技学院、西南大学动物科技学院、西南大学动物科技学院 |
| 更多格式 | 高清、无水印(增值服务) |