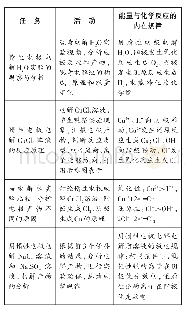
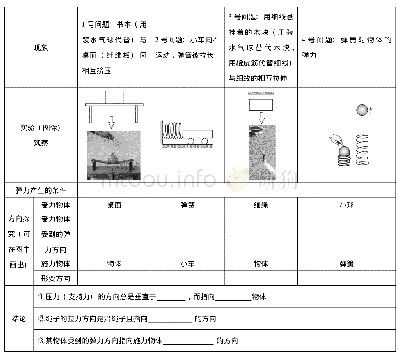
《表1 学生方案:利用传感器技术探究电解氯化钠稀溶液的实验》
为培养学生科学探究的核心化学素养[2],笔者让学生自行设计实验验证猜想,学生方案见表1。在后续实验中学生发现电解过程刚开始,在阳极附近,湿润的蓝色石蕊试纸就很快变红,但是并没有立刻褪色,学生经过讨论认为大部分氯气溶于氯化钠稀溶液中,逸出的氯气量太少导致蓝色石蕊试纸变红后没有立刻褪色。进行补充实验:用玻璃棒蘸取阳极附近液体滴在蓝色石蕊试纸上,试纸立刻被漂白,说明Cl-放电产生了氯气。湿润的淀粉碘化钾试纸在阳极附近瞬间变蓝,同样说明有氯气产生。但在阳极附近,带火星的木条一直没有复燃,难道没有氧气产生吗?经查阅资料后,发现莘赞梅[3]利用原理:O2+4H++2I-=I2+2H2O,在电解1.0 mol/L NaCl实验中检验到了氧气,方法是在电解5min时,用注射器抽取阳极气体,用Na OH浓溶液洗涤,再抽取洗涤后气体注入到淀粉KI溶液,溶液不变蓝,注入稀硫酸酸化的淀粉KI溶液,溶液变蓝。说明实验中有氧气产生。针对实验中的异常现象(带火星木条未复燃)学生猜测是氧气量太低,但需要进一步展开定量实验,而传统方法很难做到,因此笔者与学生一同利用手持技术进行了一系列探究。
| 图表编号 | XD0068388600 严禁用于非法目的 |
|---|---|
| 绘制时间 | 2019.07.25 |
| 作者 | 孙彤、朱燕 |
| 绘制单位 | 北京房山区教师进修学校 |
| 更多格式 | 高清、无水印(增值服务) |
 提示:宽带有限、当前游客访问压缩模式
提示:宽带有限、当前游客访问压缩模式