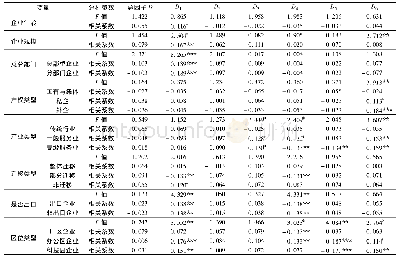
《表2 EMA认为是实质性/非实质性的临床试验期间的药学变更》
 提示:宽带有限、当前游客访问压缩模式
提示:宽带有限、当前游客访问压缩模式
本系列图表出处文件名:随高清版一同展现
《浅析国内外药品临床试验期间药学变更的监管及技术评价考虑》
注:*表示在正文中举例说明
部分EMA指导原则中对实质性/非实质性药学变更的列举见表2[13,15]。对于物质基础相差较大的不同类别药品,该表并不能统一套用。如由于化药类和生物类产品本质性不同,两者对于生产规模放大变更所伴随影响的预判和评估是不同的。化药类在进行生产规模放大时,根据产品确定的化学结构,通常有条件采用既往经验或可衡量的标准,因此,其生产规模放大具有可作为非实质性变更的理论基础。然而生物制品在进行规模放大时,产品生物学特性改变是常态化,且较难判定,因此,该类变更需综合质量可比性研究结果以确定是否作为实质性变更。
| 图表编号 | XD0041629900 严禁用于非法目的 |
|---|---|
| 绘制时间 | 2019.02.20 |
| 作者 | 金苏、李敏 |
| 绘制单位 | 国家药品监督管理局药品审评中心、国家药品监督管理局药品审评中心 |
| 更多格式 | 高清、无水印(增值服务) |