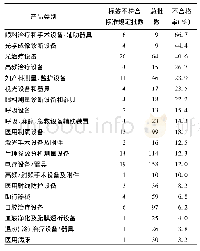
《表3 标签和说明书不符合标准规定的医疗器械分类情况(单位:批)》
 提示:宽带有限、当前游客访问压缩模式
提示:宽带有限、当前游客访问压缩模式
本系列图表出处文件名:随高清版一同展现
《基于2018—2019年国家医疗器械质量监督抽检的标签和说明书不符合标准规定情况分析》
依据《医疗器械分类规则》(原国家食品药品监督管理总局令第15号)[10],医疗器械根据结构特征的不同,可分为无源医疗器械和有源医疗器械,体外诊断试剂则单独划分。基于以上背景对2018—2019年医疗器械国抽中的不符合标准规定批次进行分析发现,标签和说明书不符合标准规定的医疗器械主要为有源医疗器械,共计149批,占标签和说明书不符合标准规定批次的98.0%;无源医疗器械共计3批(均为医用射线防护设备),占标签和说明书不符合标准规定批次的2.0%;无体外诊断试剂。经卡方检验,这三类器械的标签和说明书不符合标准规定比例差异有统计学意义(P<0.001)(见表3)。由此可见,标签和说明书问题主要涉及有源医疗器械,且在有源医疗器械总不符合标准规定批次中也占据相当大的比例。
| 图表编号 | XD00192057500 严禁用于非法目的 |
|---|---|
| 绘制时间 | 2020.12.01 |
| 作者 | 肖桂金、于淼、张薇薇、席晓宇、顾淼 |
| 绘制单位 | 中国药科大学国家药物政策与医药产业经济研究中心、国家药品监督管理局信息中心、中国药科大学国家药物政策与医药产业经济研究中心、中国药科大学国家药物政策与医药产业经济研究中心、国家药品监督管理局信息中心 |
| 更多格式 | 高清、无水印(增值服务) |