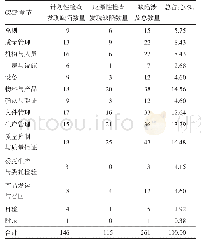
《表3 CFDI 2018年度GMP跟踪检查15大不合格条款》
 提示:宽带有限、当前游客访问压缩模式
提示:宽带有限、当前游客访问压缩模式
本系列图表出处文件名:随高清版一同展现
《英国2018年GMP检查缺陷对中国GMP实施的启示》
经统计,在质量控制与质量保证(第1 0章)、文件管理(第8章)、无菌药品附录、设备(第5章)、确认与验证(第7章)、物料与产品(第6章)、厂房与设施(第4章)、生产管理(第9章)、机构与人员(第3章)、计算机系统附录、确认与验证附录、质量管理及中药制剂附录等部分的缺陷占全部缺陷的95%,其中前8项占比81%。在质量控制与质量保证部分发现的缺陷最为突出,共554条,占全部缺陷的28%;其次是文件管理,占比15%;无菌药品附录、设备方面的缺陷占比8%。CFDI 2018年度GMP跟踪检查15大不合格条款,见表3。
| 图表编号 | XD00159945800 严禁用于非法目的 |
|---|---|
| 绘制时间 | 2020.08.20 |
| 作者 | 葛渊源、陈桂良 |
| 绘制单位 | 上海药品审评核查中心、上海药品审评核查中心 |
| 更多格式 | 高清、无水印(增值服务) |