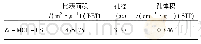《表2 200~1000K温度区间内裸反应单、三重态下的速率常数k (cm3·molecule-1·s-1) 随温度T的变化》
由前述2.2节部分内容可知,单重态下的通道R2需要克服的能垒(8.78kJ·mol-1)最低,是标题反应主通道。通道R2在计算范围内的速率常数为2.76×10-13~2.76×10-13cm3·molecule-1·s-1(表2),比R1和R3反应通道的速率常数高出了10~11个数量级。并且在298K时其速率常数(7.78×10-13cm3·molecule-1·s-1)与实验值(9.6×10-12cm3·molecule-1·s-1)相近,表明通道R2是NO2+HSO反应单重态反应势能面上的主通道。
| 图表编号 | XD0066045000 严禁用于非法目的 |
|---|---|
| 绘制时间 | 2019.06.18 |
| 作者 | 吕陇梅、耿琳、文明杰、乔张宇、寇伟华、王琰、田少博、王睿 |
| 绘制单位 | 陕西理工大学化学与环境科学学院陕西省催化重点实验室、陕西理工大学化学与环境科学学院陕西省催化重点实验室、陕西理工大学化学与环境科学学院陕西省催化重点实验室、陕西理工大学化学与环境科学学院陕西省催化重点实验室、陕西理工大学化学与环境科学学院陕西省催化重点实验室、陕西理工大学化学与环境科学学院陕西省催化重点实验室、陕西理工大学化学与环境科学学院陕西省催化重点实验室、陕西理工大学化学与环境科学学院陕西省催化重点实验室 |
| 更多格式 | 高清、无水印(增值服务) |
 提示:宽带有限、当前游客访问压缩模式
提示:宽带有限、当前游客访问压缩模式