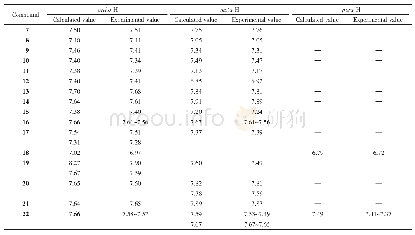
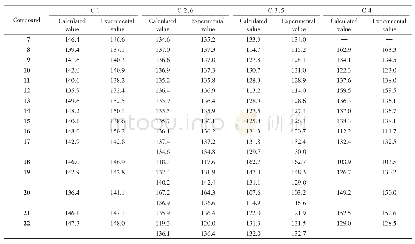
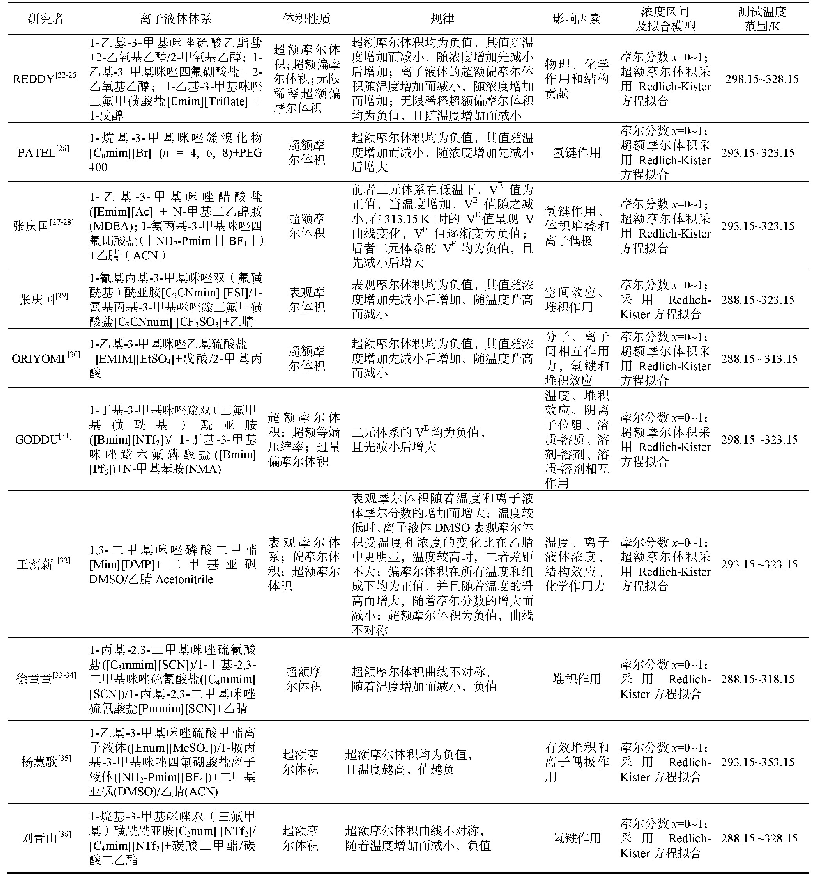
《表3 离子液体中咪唑环上C2-H的1H NMR化学位移(δ值)和计算出的相应阴离子的β值》
 提示:宽带有限、当前游客访问压缩模式
提示:宽带有限、当前游客访问压缩模式
本系列图表出处文件名:随高清版一同展现
《毛竹半纤维素在1-丁基-3-甲基咪唑型离子液体中的溶解性能》
为了进一步评估本研究中所用5种离子液体的阴离子形成氢键的能力,因此借鉴Lungwitz和Spange[34]的方法计算它们的β值,并通过β值简单评估它们形成氢键的能力,结果如表3所示。结果表明,计算获得的β值中,[CH2CHCOO]-的β值(0.85)与[H2NCH2COO]-相等,并略大于[C6H5COO]-的β值(0.83),同时[HOCH2COO]-和[CH3CHOHCOO]-的β值分别为0.76和0.78,表明[CH2CHCOO]-、[H2NCH2COO]-和[C6H5COO]-接受质子并形成氢键的能力强于[HOCH2COO]-和[CH3CHOHCOO]-。如果同时考虑溶解度测定和NMR分析的实验误差,通过计算获得的β值大小顺序与这5种ILs溶解半纤维素的能力几乎一致(图3),且与溶解半纤维素前后阴离子中C11和C12的化学位移变化幅度规律(图5)以及在ILs中溶解前后半纤维素中木糖单元上碳的化学位移变化幅度规律(图6)也几乎一致。该结果进一步表明,ILs的阴离子形成氢键能力越强,其接受半纤维素中的羟基质子并形成氢键的能力就越强,从而促进半纤维素在ILs中的溶解。
| 图表编号 | XD0064505500 严禁用于非法目的 |
|---|---|
| 绘制时间 | 2019.09.05 |
| 作者 | 袁林、彭红、何鸿伟、胡莉芳、张宇、夏琪、阮榕生、张锦胜、彭文屹、刘玉环 |
| 绘制单位 | 南昌大学生物质转化教育部工程研究中心、南昌大学材料科学与工程学院、南昌大学生物质转化教育部工程研究中心、南昌大学食品科学与技术国家重点实验室、南昌大学生物质转化教育部工程研究中心、南昌大学食品科学与技术国家重点实验室、南昌大学生物质转化教育部工程研究中心、南昌大学食品科学与技术国家重点实验室、南昌大学生物质转化教育部工程研究中心、南昌大学食品科学与技术国家重点实验室、南昌大学生物质转化教育部工程研究中心、南昌大学食品科学与技术国家重点实验室、南昌大学生物质转化教育部工程研究中心、南昌大学食品科学与技术国家 |
| 更多格式 | 高清、无水印(增值服务) |