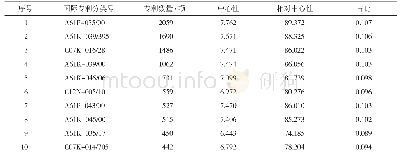
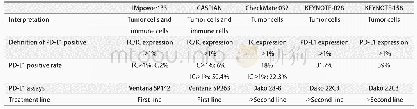
《表2 已上市PD-1/PD-L1抑制剂相关Ⅲ期临床试验结果》
 提示:宽带有限、当前游客访问压缩模式
提示:宽带有限、当前游客访问压缩模式
本系列图表出处文件名:随高清版一同展现
《PD-1/PD-L1抑制剂在晚期NSCLC免疫治疗中的应用研究进展》
注:试验组是指含试验药物组;对照组是指不含试验药物组(详见相关临床试验);-表示相关数据未成熟
基于CheckMate-017、CheckMate-057这2项Ⅲ期临床试验结果(比较Nivolumab与多西他赛),美国FDA于2015年先后批准Nivolumab用于治疗后进展的鳞癌型和非鳞癌型晚期NSCLC患者的二线治疗[16-17]。随访至今,最新数据显示Nivolumab能给患者持续的生存获益,进一步巩固其在二线治疗中的优势地位[18]。CheckMate-017、CheckMate-057这2项研究主要针对西方人群,那么东亚人群呢?吴一龙团队在中国开展的Ⅲ期临床研究(CheckMate-078)解答了这一问题。据今年4月份美国癌症研究协会会议上口头公布的结果,Nivolumab在耐受性和安全性方面与CheckMate-017、CheckMate-057研究结果一致,见表2[19]。CheckMate-078临床试验阳性结果证实,Nivolumab对东亚人群也有效果且安全性较好;其亚组研究结果显示,Nivolumab对不同肿瘤组织学类型和PD-L1表达水平的患者都有效果[19]。这有望开启中国肺癌免疫治疗的新时代。
| 图表编号 | XD0048264700 严禁用于非法目的 |
|---|---|
| 绘制时间 | 2019.01.30 |
| 作者 | 包晓燕、陈飞、金铁峰、高文仓 |
| 绘制单位 | 浙江省肿瘤医院妇科肿瘤外科、浙江省肿瘤医院妇科肿瘤外科、浙江省肿瘤医院妇科肿瘤外科、浙江中医药大学附属第二医院肿瘤科 |
| 更多格式 | 高清、无水印(增值服务) |