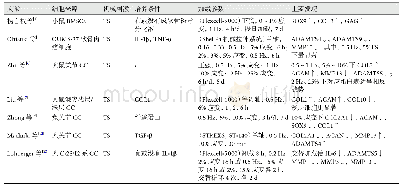
《表1 TS对体外CC代谢的影响》
注:SOX9(sex-determining region Y box 9,SRY相关蛋白9);COL2/2A1(collagen typeⅡ/ⅡA1,Ⅱ型胶原蛋白/Ⅱ型胶原蛋白α1);GAG(glycosaminoglycan,糖胺聚糖);IL-1β,IL-6(interleukin-1β,interleukin-6,白细胞介素-1β,白介素6);TNF-α(tumor necrosis factor-α,肿
牵张力(tensile strain,TS)是体内最为常见的内力,是近年来研究的热点[3]。有报道表明低强度(0~1%)应变、1 Hz的TS能够促进骨髓间充质干细胞(bone mesenchymal stem cells,BMSCs)向CC分化,且软骨形成标志物的表达随时间的延长而上调[4]。也有研究发现加载中强度(2%~10%)应变、0.16~0.5 Hz的TS可以促进CC合成[5-7]。一些学者认为这可能是通过激活单磷酸腺苷激活的蛋白激酶(adenosine monophosphate-activated protein kinase,AMPK)和抑制核因子κB(nuclear factor kappa-B,NF-κB)-p65的核转运来减轻软骨损伤[8]。但Zhong等[9]对兔CC进行10%应变的TS后,却发现CC表型被破坏,这可能与TS激活粘附斑激酶(focal adhesion kinase,FAK)-丝裂原活化蛋白激酶(mitogen-activated protein kinases,MAPK)信号,从而上调炎症因子的表达有关[10]。Liu等[7]表明在中度TS加载下,浅层CC更能维持细胞表型,延缓细胞衰老。而高强度(>10%)应变、0.5 Hz的TS常常会抑制CC表型的形成,引起基质的降解[6,11-12]。但Lohberger等[13]发现交替加载低、高强度的TS反而能够显著减少基质的降解,从而降低对CC表型的破坏。如何联合加载低、中、高强度的TS使之促进CC增殖还需要广大研究者的不断探索。关于TS对体外CC代谢的影响详见表1。
| 图表编号 | XD00208037600 严禁用于非法目的 |
|---|---|
| 绘制时间 | 2020.12.25 |
| 作者 | 杨光露、郭杨、涂鹏程、吴承杰、潘娅岚、马勇 |
| 绘制单位 | 南京中医药大学附属医院骨伤科、南京中医药大学骨伤修复与重建新技术实验室、南京中医药大学附属医院骨伤科、南京中医药大学骨伤修复与重建新技术实验室、南京中医药大学附属医院骨伤科、南京中医药大学骨伤修复与重建新技术实验室、南京中医药大学附属医院骨伤科、南京中医药大学骨伤修复与重建新技术实验室、南京中医药大学中西医结合护理研究所、南京中医药大学附属医院骨伤科、南京中医药大学骨伤修复与重建新技术实验室、南京中医药大学中医学院·中西医结合学院 |
| 更多格式 | 高清、无水印(增值服务) |
 提示:宽带有限、当前游客访问压缩模式
提示:宽带有限、当前游客访问压缩模式





