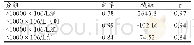《表1 3种细胞死亡方式的比较》
 提示:宽带有限、当前游客访问压缩模式
提示:宽带有限、当前游客访问压缩模式
本系列图表出处文件名:随高清版一同展现
《铁死亡相关机制与其在肝脏相关疾病中作用的研究进展》
铁死亡由Brent R.Stockwell博士于2012年命名,是一种铁依赖性的由脂质过氧化产物和活性氧(reactive oxygen species,ROS)堆积而导致的细胞调节性死亡方式[2]。铁死亡在形态学、生化特征和调控机制上与其他细胞死亡方式(如凋亡、坏死等)有所不同(表1)[3]:(1)形态学方面。细胞凋亡时表现为细胞膜无破裂,胞内出现典型的凋亡小体。细胞坏死时表现为细胞肿胀,细胞核浓缩、碎裂、溶解,染色质染色变淡、呈絮状,细胞器膨大或碎裂。铁死亡则无典型的细胞凋亡和坏死表现,主要为细胞膜破裂和出泡,线粒体萎缩,膜密度增加、嵴减少,细胞核缺乏染色质凝集等。(2)生化特征和调控机制方面。细胞凋亡过程主要依赖含半胱氨酸的天冬氨酸蛋白水解酶(cysteinyl aspartate specific proteinase,Caspase),凋亡发生时胞浆Ca2+和p H水平升高,核酸内切酶被激活导致核DNA片段化,细胞膜磷脂酰丝氨酸外翻,线粒体膜电位降低,通透性增强。细胞坏死会引起局部严重的炎症反应,与受体相互作用蛋白激酶3(receptor interacting protein kinase 3,RIPK3)等多种信号通路有关。而铁死亡时,细胞内Fe2+发生聚集,脂质过氧化水平显著升高、ROS增加,细胞半胱氨酸摄取减少、谷胱甘肽(glutathione,GSH)耗竭并释放花生四烯酸等介导因子等[4];铁死亡的实质是Fe2+累积和细胞氧化还原代谢发生紊乱,即细胞抗氧化能力下降,ROS和脂质过氧化产物在细胞内得不到还原而大量累积,进而诱导细胞死亡;其与细胞凋亡和坏死发生机制间均不存在交叉,抑制细胞凋亡、坏死的小分子对铁死亡无抑制作用[5]。
| 图表编号 | XD00206185600 严禁用于非法目的 |
|---|---|
| 绘制时间 | 2020.11.28 |
| 作者 | 贺明、魏倩、张颖婷 |
| 绘制单位 | 上海交通大学基础医学院病理生理学系细胞分化与凋亡教育部重点实验室、上海交通大学基础医学院病理生理学系细胞分化与凋亡教育部重点实验室、上海交通大学基础医学院病理生理学系细胞分化与凋亡教育部重点实验室 |
| 更多格式 | 高清、无水印(增值服务) |
![表4 两种诊断方式的细胞病理诊断组织学分型比较[n(%)]](http://bookimg.mtoou.info/tubiao/gif/ZDYS202031051_02700.gif)