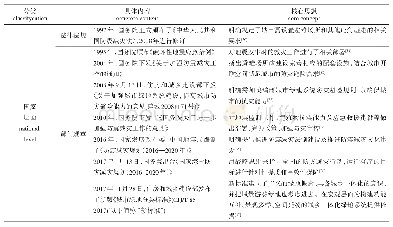
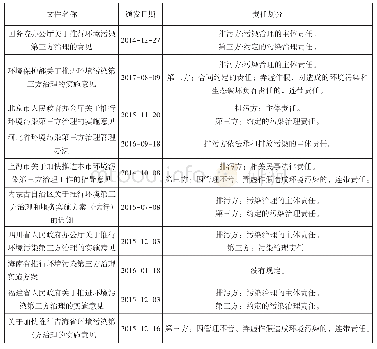
《表1 我国关于医学方面伦理治理政策文件一览表(部分)》
 提示:宽带有限、当前游客访问压缩模式
提示:宽带有限、当前游客访问压缩模式
本系列图表出处文件名:随高清版一同展现
《大科学时代我国科技伦理中待解决的问题——以“主体-工具-价值”为框架的分析》
强制性工具是政府治理科技伦理的刚性约束。涉及到伦理问题的科研活动通常广泛存在于医学、生物等和生命相关的科学领域。为了约束科技工作者的行为,需要有相应法律法规作为依据。我国对于伦理问题的监管相较于西方发达国家起步晚,1991年在中美合作的一个医学项目上,在美方要求下建立了第一个伦理委员会。随着时间的推移,伦理监管的重要性逐渐被有关部门重视,卫生部长陈敏章在1997年要求大医学单位建立伦理委员会,自此正式开启伦理审查在中国的历史。经过近三十年的发展,我国目前尚无关于伦理审查制度的国家层面立法。如表1所示,对于伦理委员会的规制分布在规范性文件为主的相关立法中,相比较于由人大及常委会制定的高位阶法律,主要由各部委制定的规范性文件呈现出以低阶立法为主要监管依据的特征。在《药物临床试验质量管理规范》等行政立法中,均涉及了对伦理委员会职权的规定,但缺少对伦理委员会监管问题的明确规定。卫计委2016年出台的《涉及人的生物医学研究伦理审查办法》,对于监管问题做了进一步规定,但也没有改变伦理委员会监管依据立法层级较低的问题。立法层次低,一方面意味着法律所赋予权力的在行使过程中,可能受到诸多因素的制约,比如来自于部门利益或是地方利益的干涉,造成治理的低效甚至无效。另一方面,层次低可能造成一些行政法规过于宽松,部委规章的性质使其无法设定民事责任等制裁手段,使得一些违反法律的行为成本不高,反倒是助长了违反科技伦理的乱象进一步滋生。
| 图表编号 | XD00201197900 严禁用于非法目的 |
|---|---|
| 绘制时间 | 2020.11.15 |
| 作者 | 刘志辉、孙帅 |
| 绘制单位 | 天津财经大学财税与公共管理学院、天津财经大学财税与公共管理学院 |
| 更多格式 | 高清、无水印(增值服务) |