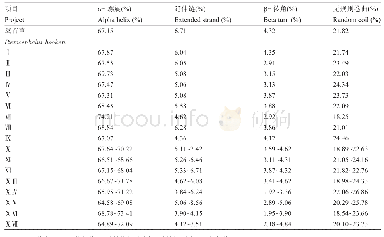
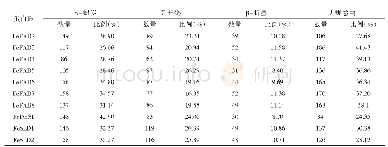
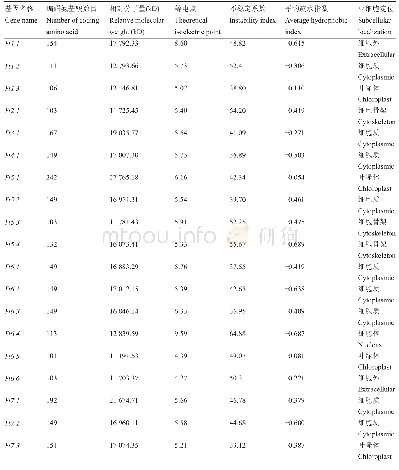
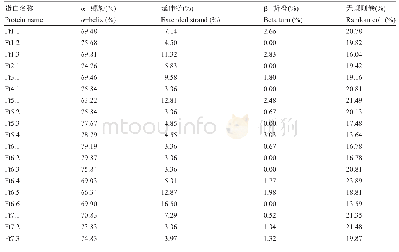
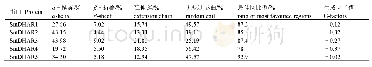《表2 苦荞14-3-3蛋白二级结构主要组件比例》
蛋白质二级结构是指多肽主链骨架原子沿一定的轴盘旋或折叠而形成的特定的构象,即肽链主链骨架原子的空间位置排布,不涉及氨基酸残基侧链。一般包括α-螺旋、β-折叠、β-转角和无规卷曲。苦荞14-3-3蛋白的β-折叠所占的比例很小,少部分不含有β-折叠,主要以α-螺旋、延伸链和无规则卷曲为主(表2;图1)。19条14-3-3氨基酸序列中,α-螺旋所占的比列最高,占63.22%~79.87%。蛋白质三级结构是在二级结构的基础上,肽链进一步折叠盘绕而形成的三维空间。根据SWISS-MODEL同源建模,初步构建的三级结构模型结果显示(图2),α-螺旋占的比例最大,其次是无规则卷曲。根据三级结构大致可以分为4组:一组为Ft3.1和Ft5.4;一组为Ft2.1、Ft5.3、Ft6.4;一组为Ft1.3、Ft5.1、Ft6.5、Ft6.6;一组为Ft4.1、Ft5.2、Ft6.1、Ft6.2、Ft6.3、Ft7.1、Ft7.2、Ft7.3。每一组的三级结构具有相似性,而组与组之间又存在差异,其二级结构的组件比例以及卷曲盘绕的程度略有不同。
| 图表编号 | XD00194461500 严禁用于非法目的 |
|---|---|
| 绘制时间 | 2021.03.14 |
| 作者 | 时兴伟、陈叶、李玉兰、袁哲明、董玉梅、李兰芝 |
| 绘制单位 | 湖南农业大学湖南省农业大数据分析与决策工程技术研究中心、湖南农业大学湖南省农业大数据分析与决策工程技术研究中心、湖南农业大学湖南省农业大数据分析与决策工程技术研究中心、湖南农业大学湖南省农业大数据分析与决策工程技术研究中心、云南农业大学省部共建云南生物资源保护与利用国家重点实验室、湖南农业大学湖南省农业大数据分析与决策工程技术研究中心 |
| 更多格式 | 高清、无水印(增值服务) |
 提示:宽带有限、当前游客访问压缩模式
提示:宽带有限、当前游客访问压缩模式