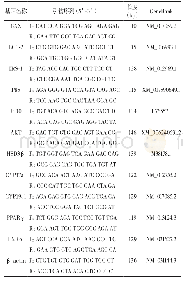
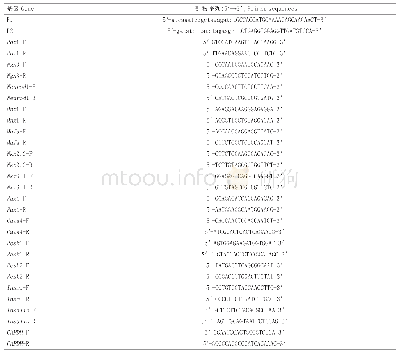
《表1 引物序列:过表达miR-202对甲状腺癌细胞恶性表型的影响及作用机制》
 提示:宽带有限、当前游客访问压缩模式
提示:宽带有限、当前游客访问压缩模式
本系列图表出处文件名:随高清版一同展现
《过表达miR-202对甲状腺癌细胞恶性表型的影响及作用机制》
2.研究方法:(1)细胞培养:甲状腺癌细胞系TPC-1和8505C购自中国科学院细胞库。所有细胞均在含有10%胎牛血清和1%青霉素-链霉素溶液的RPMI-1640培养基中培养(均购自美国Gibco公司),于37℃、5%CO2的细胞培养箱中培养。(2)细胞转染:用miR-202阴性模拟物和miR-202模拟物分别转染对数生长期的TPC-1细胞,分别命名为NC-1组和mimics-1组;用miR-202阴性模拟物和miR-202模拟物分别转染对数生长期的8505C细胞,分别命名为NC-2组和mimics-2组;对miR-202模拟物成功转染的TPC-1和8505C细胞,进行ROCK1表达载体转染,命名为mimics+ROCK1组。所有转染均使用Lipofectamine 2000(美国Invitrogen公司),操作严格按照Lipofectamine 2000说明书进行。(3)实时荧光定量聚合酶链式反应技术(quantitative real time polymerase chain reaction,qRT-PCR实验):使用TRIzol试剂(美国Invitrogen公司)提取组织中的总RNA,使用逆转录试剂盒(美国Invitrogen公司)合成互补DNA(cDNA)。qRT-PCR实验采用20μl反应系统,其中cDNA(1μl),正向引物(1μl)和反向引物(1μl)。扩增反应过程为变性(95℃,10s)、退火(60℃,20s)和延伸(72℃,30s)三个步骤。扩增循环数为40,采用2-ΔΔCt分析数据。以U6为内参。miR-202和U6引物序列见表1。(4)双荧光素酶报告实验:通过靶扫描检测ROCK1是否为miR-202的直接靶基因,并确定靶结合位点。基于结合位点设计ROCK1靶序列,通过PCR反应扩增该片段并插入到psi CHECK-2载体中。miR-202目标序列,包括突变和野生(MT和WT)序列,也分别插入到psi CHECK-2报告载体中。miR-202模拟物与mt-psiCHECK-2报告载体或wt-psiCHECK-2报告载体分别使用Lipofectamine 2000试剂共转染TPC-1和8505C细胞,培养48h后,通过双荧光素酶报告基因检测系统(北京普洛麦格公司)检测各组细胞的荧光素酶相对表达强度。(5)CCK8实验:经过0、12、24和36h培养,将装有细胞的96孔板取出并在每个孔中加入10μl CCK8溶液和90μl的细胞培养基,后将细胞在37°C下避光孵育1h,450nm波长下测定各孔吸光度(OD450值)。(6)Caspase-3酶联免疫吸附试验(武汉华美公司):将细胞反复冻融破坏细胞膜后,离心取上清。取100u样品加入预包被Caspase-3抗体的酶标板,孵育30min,加入辣根过氧化物酶标记的抗Caspase-3抗体,后用底物显色,酶标仪测定OD450值。
| 图表编号 | XD00142089500 严禁用于非法目的 |
|---|---|
| 绘制时间 | 2020.03.20 |
| 作者 | 吴恢升、吴妹、曾海勇、王先明 |
| 绘制单位 | 深圳大学第一附属医院甲乳外科、深圳大学第一附属医院高压氧科、深圳大学第一附属医院内分泌科、深圳大学第一附属医院甲乳外科 |
| 更多格式 | 高清、无水印(增值服务) |