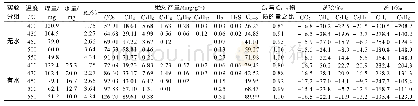
《表1 8个双[1]轮烷产率及核磁对比》
![《表1 8个双[1]轮烷产率及核磁对比》](http://bookimg.mtoou.info/tubiao/gif/YJHU201912016_01100.gif) 提示:宽带有限、当前游客访问压缩模式
提示:宽带有限、当前游客访问压缩模式
本系列图表出处文件名:随高清版一同展现
《基于柱[5]芳烃的新型双-[1]轮烷的设计与合成》
双[1]轮烷3a~3h通过1H NMR、13C NMR、2D NMR(1H-1H NOESY NMR)、IR和高分辨质谱MS等手段进行表征.在席夫碱桥联双柱[5]芳烃3a~3h的1H NMR谱图的负场方向,可以明显观察到一些信号峰.8种双[1]轮烷在负场方向氢的个数如表1所示.图1表示3a在CDCl3中的1H NMR谱,根据负场中的质子数,将它们归属于3a的胺基烷烃链上质子H1-4,由于相应的CH2受到柱芳烃空腔的电子云的屏蔽作用从而使化学位移向高场移动(Δδ=-0.07~-2.27),这说明两个胺基烷烃链穿入柱芳烃的两个空腔中,表明形成了[1]轮烷.这一结论是与我们课题组之前合成的基于单酰胺功能化柱[5]芳烃的[1]轮烷所得结论一致[29].在2D NOESY NMR图谱(图2)中,明显观察到己基质子H1-4与3a的柱[5]芳烃侧链亚甲基质子Ha(图2,A、B、C、D)、H1-4与NH质子Hb(图2,E、F)以及H1-4与苯环质子Hc(G、H、I、J)之间存在明确的相关信号,这也证实了烷基链穿入柱芳烃空腔中,形成了双-[1]轮烷的机械互锁结构.其他7个基于柱芳烃的双-[1]轮烷同样通过以上手段进行表征.通过对比发现双-[1]轮烷中氢在δ0以下出峰的位置和个数与烷基二胺的链长n有关,进一步说明柱芳烃套在烷基二胺的烷基链上.
| 图表编号 | XD00126044900 严禁用于非法目的 |
|---|---|
| 绘制时间 | 2019.12.01 |
| 作者 | 张润淼、王陈威、孙晶、颜朝国、姚勇 |
| 绘制单位 | 扬州大学化学化工学院、南通大学化学化工学院、南通大学化学化工学院、扬州大学化学化工学院、扬州大学化学化工学院、南通大学化学化工学院 |
| 更多格式 | 高清、无水印(增值服务) |

![表1 在不同溶剂中形成[2]准轮烷的键合常数Ka/103M-1[a]对比[32]](http://bookimg.mtoou.info/tubiao/gif/HXJZ202011003_42100.gif)
![表1:两组产妇早产率及剖宫产率比较[n(%),n=47]](http://bookimg.mtoou.info/tubiao/gif/ZGCF202005106_02000.gif)

![表1 不同结构的聚轮烷比较[47]](http://bookimg.mtoou.info/tubiao/gif/HGJZ202006008_01000.gif)