《表6 干细胞临床研究方案中伦理和实施情况分析》
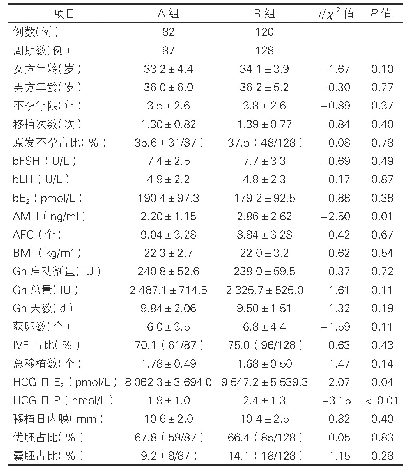
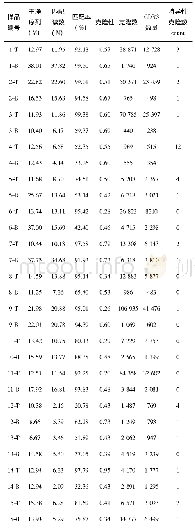
干细胞临床研究方案除了满足科学性要求外,还须符合《涉及人的生物医学研究伦理审查办法(试行)》和《人胚胎干细胞研究伦理指导原则》的要求,保证受试者的权益得到充分尊重和保护。表6中显示仅有19项(6.91%)研究明确说明设立数据与安全监察委员会,10.80%方案无不良事件的定义与记录方式,19.92%的方案未明确严重不良事件的报告与处理方法,且仅有15.53%的方案涉及到伦理委员会审批相关内容。干细胞类治疗为相对风险较高的项目,研究者应当采取有效措施为受试者提供相应保障,干细胞临床研究更应从研究方案的源头上加强关于受试者权益保护与风险控制措施。
| 图表编号 | XD0087929000 严禁用于非法目的 |
|---|---|
| 绘制时间 | 2019.06.10 |
| 作者 | 谢丽、路茂杰、沈力、宋雪霏、吴朝晖、钱碧云 |
| 绘制单位 | 上海交通大学医学院临床研究中心、上海交通大学医学院公共卫生学院、上海交通大学医学院公共卫生学院、上海交通大学医学院附属第九人民医院眼科、中国医药生物技术协会、上海交通大学医学院临床研究中心 |
| 更多格式 | 高清、无水印(增值服务) |
 提示:宽带有限、当前游客访问压缩模式
提示:宽带有限、当前游客访问压缩模式