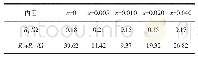
《表3 淬火样品x Li2MnO3- (1-x) Li[Ni0.8Co0.15Al0.05]O2 (0.5≤x≤0.8) 在电流密度为20 mA·g-1的首次充放电电化学数据》
![《表3 淬火样品x Li2MnO3- (1-x) Li[Ni0.8Co0.15Al0.05]O2 (0.5≤x≤0.8) 在电流密度为20 mA·g-1的首次充放电电化学数据》](http://bookimg.mtoou.info/tubiao/gif/WJHX201906001_03600.gif) 提示:宽带有限、当前游客访问压缩模式
提示:宽带有限、当前游客访问压缩模式
本系列图表出处文件名:随高清版一同展现
《xLi_2MnO_3-(1-x)Li[Ni_(0.8)Co_(0.15)Al_(0.05)]O_2(0.5≤x≤0.8)的结构和电化学性能》
图5(a)为室温下x Li2MnO3-(1-x)Li[Ni0.8Co0.15Al0.05]O2(0.5≤x≤0.8)在电流密度为20 m A·g-1,电压范围为2.0~4.8 V时的首次充放电曲线图。由图可知,对于所有样品的充电曲线图都分为2部分:(1)在<4.5V时,Li+离子从Li[Ni0.8Co0.15Al0.05]O2层脱出并伴随Ni2+/Ni4+和Co3+/Co4+的氧化反应;(2)在>4.5 V时,Li2MnO3层脱出Li+并释放O2-,形成Li2O,发生不可逆反应导致较高的不可逆的电化学容量损失[20-21]。从表3和4可以看出,相同组分的淬火样品的首圈放电比容量以及首圈库伦效率都比未淬火的样品高,表明对样品进行的淬火处理能够显著改善样品的电化学性能。这是因为淬火能够导致晶粒内部微观结构和元素的价态产生较为复杂的变化,这些变化能够有助于Li2MnO3的活化,从而使得样品表现出较好的电化学性能。此外,样品的放电比容量呈现出先升高后下降的特点,这是由于放电比容量容量的起初升高主要来自于Li2MnO3的贡献,但Li2MnO3的导电性能很差,当x超过0.7时,材料的总体导电性就变得非常差了,进而妨碍了锂离子的脱嵌进程。图5(b)是室温下x Li2MnO3-(1-x)Li[Ni0.8Co0.15Al0.05]O2(0.5≤x≤0.8)在电压区间2.0~4.8 V,电流密度为20m A·g-1下循环100圈的循环图。从图中可以看出,淬火样品和未淬火样品在循环过程中的放电比容量逐渐增加,淬火样品从x=0.5、0.6、0.7、0.8时的178.2、188.9、155.8和106.3 m Ah·g-1,循环100圈后分别达到181.4、209.2、192.7和206.8 m Ah·g-1。未淬火样品从x=0.5、0.6、0.7、0.8的161.7、169.6、97.1和87.8 m Ah·g-1,循环100圈后分别达到182.1、204.2、202.4和202.9 m Ah·g-1。这种现象可能是因为在循环过程中随着锂离子的嵌入嵌出,样品中的Li2MnO3逐渐活化造成的。Li2MnO3的含量越高,这种现象越明显,一般称此活化过程为电化学活化。从图5(c,d)中可以得出,淬火样品的首次放电比容量和库伦效率都明显比未淬火样品高,其中x=0.6的淬火样品的首圈放电比容量和首圈库伦效率最高,分别达到188.9 m Ah·g-1和67.1%。而在未淬火的样品中,x=0.6的未淬火样品的首圈放电比容量和首圈库伦效率也最高,分别为169.6 mAh·g-1和58.0%。
| 图表编号 | XD0077758600 严禁用于非法目的 |
|---|---|
| 绘制时间 | 2019.06.10 |
| 作者 | 陈培雷、黄继春、陈亦新、季崇星、朱德澄、李德成 |
| 绘制单位 | 苏州大学能源学院、苏州大学能源学院、苏州大学能源学院、苏州大学能源学院、苏州大学能源学院、苏州大学能源学院 |
| 更多格式 | 高清、无水印(增值服务) |




![表1 Li[NixCoyMnz]O2(x=1/3,0.5,0.6,0.7,0.8和0.85)的I(003)与I(104)比值](http://bookimg.mtoou.info/tubiao/gif/GDHG202016034_02600.gif)