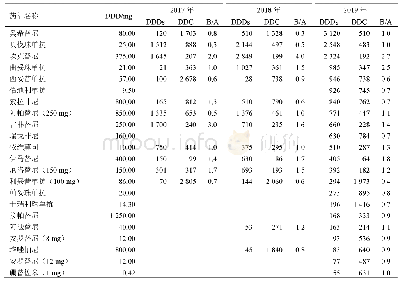
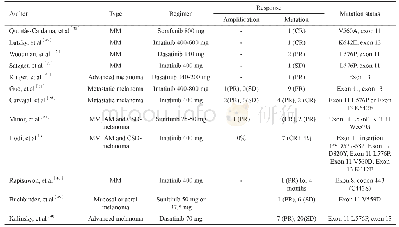
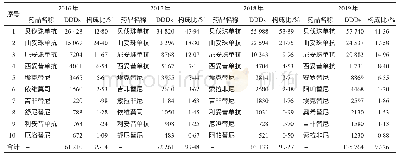
《表3 靶向实体肿瘤TCR-T治疗的研发进展》
研究人员应用TCR-T疗法对多种实体瘤(黑色素瘤、滑膜肉瘤、食管癌等)进行了研究。MORGAN等[3]学者,在体外将针对MART-127-35、gp100209-217、NYESO-1157-165、p53264-272多肽表位的TCR m RNA通过电转染的方法导入到CD8+外周血T淋巴细胞,获得抗原特异性TCR-T后,与负载了相应抗原多肽且HLA分型一致的T2细胞共培养,检测T细胞经活化产生的IFN-γ,结果显示这些TCR具有抗原识别特异性和HLA限制性。同时,作者将识别MART-1抗原的TCR-T分别回输17例处于进展期的转移性黑色素瘤患者,治疗后有2例患者显示其转移的黑色素瘤的持续客观消退。2010年,ROBBINS等[4]学者首次开展靶向NY-ESO-1的自体TCR-T治疗转移性黑色素瘤和滑膜细胞肉瘤的临床试验,回输大于1×109个特异性TCR-T细胞治疗17例肿瘤患者,结果显示6例滑膜细胞肉瘤患者中有4例患者有临床反应,1例患者身上观察到持续18个月的部分反应;表达NY-ESO-1黑色素瘤的11例患者中有5例有临床反应,且有2例表现出1年后仍持续完全消退。2015年,KAGEYAMA等[5]报道了对表达MAGE-A4抗原的复发性食管癌患者进行的TCR-T的临床试验。将10例复发性食管癌患者分3组,第一组3例每例回输2×108个特异性TCR-T细胞,第二组4例每例回输1×109个TCR-T细胞,第三组3例每例回输5×109个的TCR-T细胞。经TCR-T细胞治疗发现,10例食管癌患者中有5例外周血虽然连续五个月均检测到TCR-T细胞,但未见肿瘤明显消退,究其原因可能是该试验过程未对患者的淋巴细胞做去势处理。因此,随后的研究不仅聚焦于针对各种肿瘤靶点的TCR设计,还在临床研究方案的设计上进行探索。新的TCR-T的研究不断涌现,成为实体瘤细胞免疫治疗的主力军。根据美国Clinical Trials.gov网站登记收录,已经完成的靶向实体肿瘤TCR-T临床试验(表1)有13个,正在招募的临床试验(表2)有14个,随着对TCR-T过继免疫治疗的临床试验评估,为难治性肿瘤患者带来缓解的希望。基于TCR-T的良好应用前景,许多国内外公司参与TCR-T的研发(表3)。
| 图表编号 | XD00229187200 严禁用于非法目的 |
|---|---|
| 绘制时间 | 2020.09.25 |
| 作者 | 叶春梅、叶韵斌 |
| 绘制单位 | 福建省肿瘤转化医学重点实验室、福建省肿瘤转化医学重点实验室 |
| 更多格式 | 高清、无水印(增值服务) |
 提示:宽带有限、当前游客访问压缩模式
提示:宽带有限、当前游客访问压缩模式