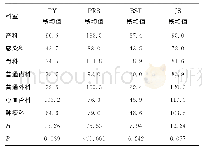
《表1 不同国家地区NSCLC患者PD-L1检测试剂和检测平台获批情况》
 提示:宽带有限、当前游客访问压缩模式
提示:宽带有限、当前游客访问压缩模式
本系列图表出处文件名:随高清版一同展现
《非小细胞肺癌PD-L1免疫组织化学检测规范中国专家共识》
“/”代表未获批;TPS:肿瘤比例评分;TC:肿瘤细胞;IC:免疫细胞;LDT:实验室自建检测;FDA:美国食品药品监督管理局;CE:欧盟;NMPA:国家药品监督管理局。PD-L1:programmed cell death-ligand 1.NSCLC:non-small cell lung cancer.
随着PD-1/PD-L1免疫检查点抑制剂获批,NSCLC患者PD-L1免疫组化检测试剂等也随适应证需要作为伴随诊断或补充诊断而相应获批[3,4]。其中最大特点是各个药物分别对应不同的PD-L1试剂克隆或平台,且其判读阈值也各不相同[5]。表1汇总了FDA、CE认证和NMPA对NSCLC患者免疫治疗时所需使用PD-L1检测试剂和检测平台的获批情况(截止2020年5月31日)。本共识建议选择我国NMPA批准的免疫组化检测试剂盒或抗体试剂,具体推荐内容详见表1。
| 图表编号 | XD00220327100 严禁用于非法目的 |
|---|---|
| 绘制时间 | 2020.09.20 |
| 作者 | PD-L1检测共识专家组 |
| 绘制单位 | PD-L1检测共识专家组 |
| 更多格式 | 高清、无水印(增值服务) |


![表1 人细小病毒B19核酸检测试剂国家参考品PCR扩增及测序引物[6]](http://bookimg.mtoou.info/tubiao/gif/YXYQ202012003_01000.gif)