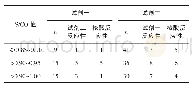
《表1 NSCLC检测PD-L1试剂及获批情况》
PD-L1检测作为补充诊断,并非治疗药物决策所必需,即使缺乏PD-L1检测结果亦可进行治疗。但PD-L1检测可以提供个体治疗的相关信息,因而可以协助筛选免疫治疗的潜在获益人群。美国FDA批准nivolumab用于以铂类药物为基础化疗方案的进展晚期鳞状或非鳞状NSCLC;批准atezolizumab用于接受含铂药物的化疗方案治疗期间或治疗后疾病进展及接受靶向治疗失败的转移性NSCLC。尽管nivolumab及atezolizumab二线治疗NSCLC均无需考虑PD-L1的表达状态,但研究结果均显示,PD-L1表达水平越高,临床获益越大,因此在一定程度上PD-L1的检测结果可辅助临床选择更适宜免疫治疗的潜在人群。随着PD-1/PD-L1免疫检查点抑制剂获批,NSCLC患者肺癌组织PD-L1检测试剂也因适应证需要而相应获批[18]。但各个药物分别对应不同的PD-L1试剂或平台,且其阈值也各不相同(表1)。
| 图表编号 | XD00215223600 严禁用于非法目的 |
|---|---|
| 绘制时间 | 2020.10.30 |
| 作者 | 李媛 |
| 绘制单位 | 复旦大学附属肿瘤医院病理科,复旦大学上海医学院肿瘤学系 |
| 更多格式 | 高清、无水印(增值服务) |
 提示:宽带有限、当前游客访问压缩模式
提示:宽带有限、当前游客访问压缩模式
![表1 2015-2017年柳州市无偿献血标本的两种ELISA试剂检测结果情况统计[n(%)]](http://bookimg.mtoou.info/tubiao/gif/JYYL202018036_01400.gif)