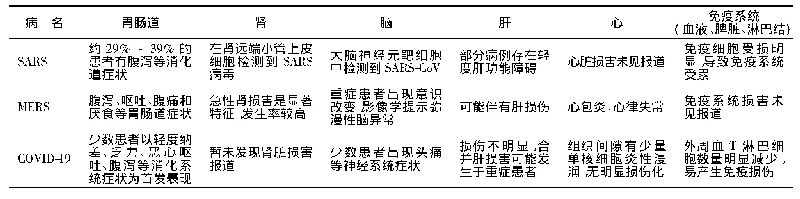
《表3 SARS、MERS、COVID-19的肺外器官损伤的病理生理变化》
 提示:宽带有限、当前游客访问压缩模式
提示:宽带有限、当前游客访问压缩模式
本系列图表出处文件名:随高清版一同展现
《SARS MERS及COVID-19的临床特点和器官损伤研究进展》
部分患者出现消化功能紊乱,重症可发生心脏、免疫系统及多器官功能障碍[30]。Wu和Mcgoogan[31]对中国44 672例确诊病例进行研究,共有4.2%的患者合并心血管疾病,12.8%的患者合并高血压。22.7%的死亡病例有心血管疾病病史,39.7%有高血压病史,提示合并心血管疾病可能是COVID-19患者预后不良的重要危险因素。而尸检病理结果显示心脏组织间隙中仅有少量细胞单核炎性浸润,无明显的病理变化。临床常见由于呼吸道感染增加心脏负担,在伴有心脏基础疾病时,诱发心功能不全甚至心力衰竭。即使病理检查未对心肌的结构损伤提供支持,考虑部分病例发生心肌炎、心力衰竭与不良预后关联密切,也应重视保护心功能。研究显示患者外周血CD4+T和CD8+T细胞的数量大大减少。但CD4+T细胞中的CCR6+Th17增多,CD8+T细胞具有高浓度的细胞毒性颗粒,T细胞呈现过度激活状态,提示发生严重的免疫系统损伤[32]。《新型冠状病毒肺炎诊疗方案(试行第七版)》中显示:脾脏明显缩小。淋巴细胞数量明显减少,灶性出血和坏死,脾脏内巨噬细胞增生并可见吞噬现象;淋巴结淋巴细胞数量较少,可见坏死。免疫组化染色显示脾脏和淋巴结内CD4+T和CD8+T细胞均减少。骨髓三系细胞数量减少。肝脏体积增大,暗红色。肝细胞变性、灶性坏死伴中性粒细胞浸润;肝血窦充血,汇管区见淋巴细胞和单核细胞细胞浸润,微血栓形成。胆囊高度充盈。Zhang等[33]的研究,在感染COVID-19后,肝脏异常的发生率显著增加,提示SARS-Co V-2可能对肝脏直接具有损伤作用或由于药物治疗的副作用所致,但目前尚无确凿证据支持。研究认为合并肝损害更有可能是重症患者药物不良反应和全身炎症所致[34],应加强肝功能监测和评估。武汉大学中南医院研究[35]显示,10.1%患者最初出现腹泻和恶心,可能与胃肠道存在病毒受体ACE-2或病毒通过损伤免疫系统进而播散至胃肠道有关。见表3。
| 图表编号 | XD00218796900 严禁用于非法目的 |
|---|---|
| 绘制时间 | 2021.01.30 |
| 作者 | 骆亚莉、王碧雯、安方玉、汪永锋、刘永琦 |
| 绘制单位 | 甘肃中医药大学基础医学院、甘肃中医药大学基础医学院、甘肃中医药大学基础医学院、甘肃中医药大学基础医学院、甘肃中医药大学基础医学院 |
| 更多格式 | 高清、无水印(增值服务) |
![表5-3 IFNα用于MERS、SARS、COVID-19治疗方案[31,40-41]](http://bookimg.mtoou.info/tubiao/gif/YAXU202010002_41000.gif)

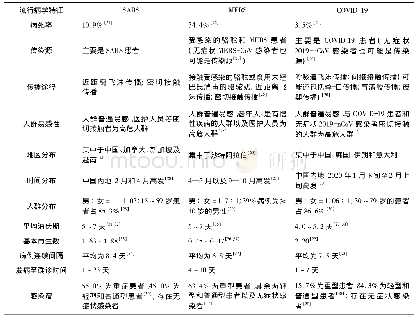
![表1 SARS、MERS和COVID-19的临床发病特点[1~5]](http://bookimg.mtoou.info/tubiao/gif/ZYLN202101024_00400.gif)
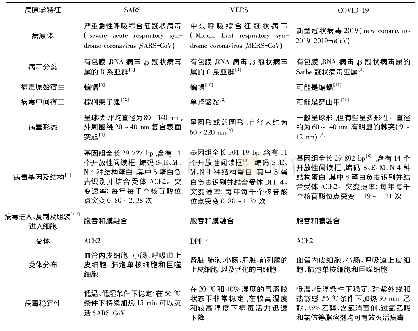
![表2 SARS、MERS、COVID-19的肺损伤比较[6,10,12~15]](http://bookimg.mtoou.info/tubiao/gif/ZYLN202101024_01200.gif)