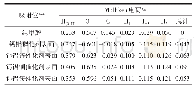
《表2 催化剂的巴德电荷分析》
为了研究S原子掺杂对Fe N4催化剂电子结构的影响,我们计算了五个研究结构的巴德电荷.巴德电荷分析如表2所示.Fe N4结构中铁原子的电子转移数为1.08|e|,引入一个S原子后Fe原子的电子转移数变为1.05|e|.引入两个S原子后,Fe原子向周围转移1.02|e|的电子数,在Fe NS3结构中,Fe原子向周围转移的电子数为0.90|e|,但是在Fe NS4结构中,Fe原子失去的电子数为1.14|e|,高于在其他结构中的电子转移数,因而,在Fe NS4结构中,Fe的价态高于Fe N4中Fe的价态.接下来,我们进一步利用电子态密度分析Fe原子与周围配位环境的成键情况,如图2所示.因为在实际成键过程中起主要作用的是最外层的电子,所以对于Fe原子而言,只考虑其3d轨道,对于N原子和S原子而言,只考虑其2p轨道.结果表明,Fe N4催化剂表面Fe原子3d轨道的电子密度较大,且Fe原子的3d轨道发生明显的电子自旋现象,由于轨道强相互作用,其自旋向上的轨道向费米能级以下偏移了大约2.0 e V,导致在费米能级附近只有自旋向下的轨道,而且此自旋向下的轨道在费米能级处的带隙为0.907 e V.引入一个S原子掺杂后,催化剂的带隙明显降低,在Fe NS1a中,带隙为0.449 e V.引入S原子的2p轨道,没有引起Fe原子的3d轨道杂化,但是会降低催化剂能带的带隙.引入更多S原子时,能带结构表现出同样的规律,Fe NS2催化剂的带隙为0.351e V,Fe NS3催化剂的带隙为0.254 e V,Fe NS4催化剂的带隙为0.121 e V.电子态密度及能带分析表明,Fe N4催化剂掺杂S原子的比例越高,催化剂电子结构的带隙变得越窄从而增强催化剂导电能力,在电催化的过程中更有利于电子的转移,因此,在Fe N4催化剂中引入S原子可以显著提高催化剂的电子转移速率.
| 图表编号 | XD00195240700 严禁用于非法目的 |
|---|---|
| 绘制时间 | 2020.09.15 |
| 作者 | 鲁效庆、曹守福、魏晓飞、李邵仁、魏淑贤 |
| 绘制单位 | 中国石油大学材料科学与工程学院、中国石油大学材料科学与工程学院、中国石油大学材料科学与工程学院、中国石油大学材料科学与工程学院、中国石油大学材料科学与工程学院 |
| 更多格式 | 高清、无水印(增值服务) |
 提示:宽带有限、当前游客访问压缩模式
提示:宽带有限、当前游客访问压缩模式

![表2 Li7Ti5O12中Ti离子的Bader电荷分析[3]](http://bookimg.mtoou.info/tubiao/gif/HNSF202004001_03700.gif)