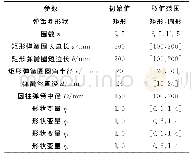
《表1 不同均质方式所制备的初始乳液的电位值和AP%值》
注:a~e为纵向显著性对比,f~g为横向显著性对比。
结合图4a和表1可知,微乳滴的粒径逐渐减小同时对应处理的AP%随之增大,故认为制备初始乳液的均质能量是不同的。图4a显示HS、US-57 W初始乳液粒径呈多峰分布,其他3种则是单峰分布,放置20d后,乳液粒径有略微增大,其中超声制备的样品曲线右移较明显,而HS的样品则是因为20 d出现油水分层现象,不符合仪器测量条件。由图4b可知,HS的样品是用30000 r/min高速均质制备出的初始乳液(油滴粒径d3,2=5.59μm,d4,3=17.60μm),并不能有效提升HIPEs的储藏稳定性。而只有采用超声或高压微射流后所制备的初始乳液,即微乳滴在d3,2=1.06μm,d4,3=2.16μm以下时,才能有效提升HIPEs的储藏稳定性。图4c是选取了两个比较代表性的HIPEs即US-570 W、MF-80 MPa室温储藏20 d前后的流变特征,发现后者的G’比前者要低些。放置20 d后,两者的G’对频率变化的依赖程度减小,即以弹性为主的凝胶网络结构有所增强。再由图4d、e分析可得,超声和微射流处理的HIPEs的大乳滴的间隙中填充和附着着密密麻麻的微乳滴(红色箭头指示),而一步乳化法和HS的则没有。再来看表1,zeta电位值在没有静电屏蔽的条件下,主要呈现出随乳液粒径的减小而增大的趋势,但在50 m M的Na Cl溶液中电位值显著下降且下降后的电位值的差异没有显著性。因此结合图3说明这些粒径小到一定程度的微乳滴的存在是提升HIPEs稳定性的重要原因。
| 图表编号 | XD00186385300 严禁用于非法目的 |
|---|---|
| 绘制时间 | 2020.11.20 |
| 作者 | 张莉丽、唐传核 |
| 绘制单位 | 华南理工大学食品科学与工程学院、华南理工大学食品科学与工程学院 |
| 更多格式 | 高清、无水印(增值服务) |
 提示:宽带有限、当前游客访问压缩模式
提示:宽带有限、当前游客访问压缩模式