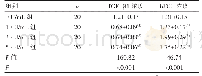
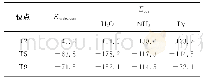
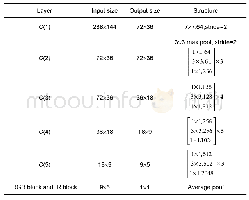
《表1 识别Aβ纤维和斑块的近红外探针》
 提示:宽带有限、当前游客访问压缩模式
提示:宽带有限、当前游客访问压缩模式
本系列图表出处文件名:随高清版一同展现
《识别β-淀粉样蛋白多样化聚集态的近红外荧光探针研究进展》
Aβ纤维的主要结构特点是富含β-片层的结构,其中单个β链定向垂直于原纤维轴。Aβ42中,C-末端β链在G37G38处弯曲,使A42接触M35的侧链;在Aβ40模型中,F19与L34接触,Q15与V36接触,H13与V40接触,两者氨基酸折叠方式虽然不同,但在这两种纤维结构中,β-转角-β单元以平行的方式排列,构象大致相同[28]。Th T是目前最为常用的识别Aβ纤维的探针,该探针与Aβ纤维表面的疏水槽结合,该疏水槽是由交叉β-片层结构重复排列而形成的[68]。Th T与Aβ纤维结合后,扭曲的分子内电荷转移受阻,非辐射跃迁被抑制[69]。与Th T结合Aβ纤维的机理类似,刚果红及其衍生物也识别Aβ纤维表面的疏水槽[70]。近年报道的识别Aβ纤维和斑块的近红外荧光探针及其结合方式归纳如下表(表1),除了以结合β-片层结构为主要互作方式外,尚缺乏探针与Aβ纤维的其他结合模式的实验数据和相关报道。
| 图表编号 | XD00182431100 严禁用于非法目的 |
|---|---|
| 绘制时间 | 2020.07.01 |
| 作者 | 刘晓慧、张菁菁、章海燕 |
| 绘制单位 | 中国科学院大学、中国科学院上海药物研究所、中国科学院大学 |
| 更多格式 | 高清、无水印(增值服务) |