《表1 国外药典标准比较表》
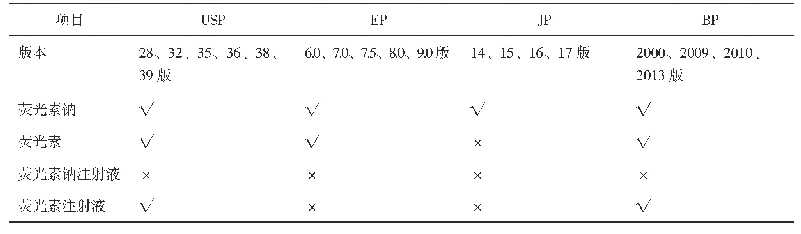
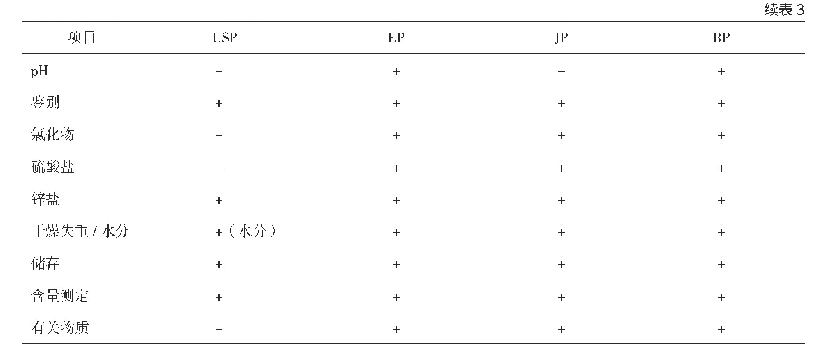
2015年版《中华人民共和国药典》仅在制剂通则部分收载了植入剂,规定了植入剂应进行释放度测定,植入剂应单剂量包装,包装容器应灭菌,植入剂应避光密封贮存,除另有规定外,还应做装量差异检查和无菌检查[1]。2019年版英国药典和42版美国药典分别收载了3.6 mg和10.8 mg 2个规格醋酸戈舍瑞林植入剂[2-3],我国进口的2个规格植入剂分别对应各版进口注册标准[4-7],其中3.6 mg规格进口注册标准进行过2次修订,主要增订了对含氧连接的戈舍瑞林二聚体的控制和溶出度28天限度,10.8 mg规格进口注册标准未进行过修订。BP 2019和USP 42中质控项目比较见表1。进口注册标准与国外药典有关物质、溶出度、含量测定等限度基本一致,部分项目具体操作存在一定差异。
| 图表编号 | XD00177374200 严禁用于非法目的 |
|---|---|
| 绘制时间 | 2020.06.30 |
| 作者 | 吕晶、郑璐侠、陈钢、邵泓 |
| 绘制单位 | 上海市食品药品检验所、上海市食品药品检验所、上海市食品药品检验所、上海市食品药品检验所 |
| 更多格式 | 高清、无水印(增值服务) |
 提示:宽带有限、当前游客访问压缩模式
提示:宽带有限、当前游客访问压缩模式